Перейти к:
Гранулематоз Вегенера: трудности диагностики и лечения
https://doi.org/10.21886/2712-8156-2023-4-4-95-100
Аннотация
Гранулематоз с полиангиитом (гранулематоз Вегенера, ГПА) — это редкое заболевание неустановленной этиологии с полиорганными поражениями, характеризующееся развитием некротизирующего гранулематозного воспаления и признаками васкулита аутоиммунного генеза, поражающего преимущественно сосуды малого и среднего калибра. В приведённом клиническом случае у пациента отмечается классическая триада симптомов (поражение верхних дыхательных путей, лёгких, почек), диагноз подтверждён морфологически. Особенностью описанного клинического случая является его редкая распространённость, сложность в постановке диагноза в связи с полиорганностью поражения, отсутствием специфических признаков в дебюте заболевания, что потребовало проведения дифференциального диагноза. Раннее определение антинейтрофильных цитоплазматических антител (АНЦА) в крови повышает частоту диагностики ГПА, а своевременное установление диагноза позволяет как можно раньше назначить терапию и избежать инвалидизации пациентов.
Ключевые слова
Для цитирования:
Баранова Ю.Р., Романова И.А., Стешенко Р.Н., Мелехина И.Ф., Никитина Н.М., Кароли Н.А. Гранулематоз Вегенера: трудности диагностики и лечения. Южно-Российский журнал терапевтической практики. 2023;4(4):95-100. https://doi.org/10.21886/2712-8156-2023-4-4-95-100
For citation:
Baranova Y.R., Romanova I.A., Steshenko R.N., Melehina I.F., Nikitina N.N., Karoli N.A. Wegener's granulomatosis: difficulties in diagnosis and treatment. South Russian Journal of Therapeutic Practice. 2023;4(4):95-100. (In Russ.) https://doi.org/10.21886/2712-8156-2023-4-4-95-100
В 30-х годах прошлого столетия немецкий патолог Friedrich Wegener объединил в триаду гранулематозный васкулит верхних и нижних дыхательных путей, системный васкулит и локальный некротизирующий гломерулонефрит [1]. Впоследствии триада была названа гранулематозом Вегенера, а позднее — гранулематозом с полиангиитом (ГПА). ГПА — гигантоклеточный гранулематозно-некротизирующий васкулит, ассоциированный с выработкой аутоантител (антител к цитоплазме нейтрофилов) и характеризующийся сочетанным воспалительным поражением нескольких органов (чаще всего верхних дыхательных путей, органов зрения и слуха, л`гких и почек) [2]. Относится к группе АНЦА-ассоциированных системных васулитов [3]. АНЦА (антинейтрофильные цитоплазматические антитела) — семейство антител, направленных против компонентов первичных гранул цитоплазмы нейтрофилов и моноцитов, которые классифицируются по типу свечения при реакции непрямой иммунофлюоресценции. В настоящее время этиология ГПА неизвестна, предполагается связь начала болезни с воздействием инфекционного агента. Патогенез заболевания связан с развитием распространённого воспаления мелких сосудов и одновременным формированием периваскулярных и экстравазальных гранулем макрофагального типа с клетками Лангханса в пораженных органах и тканях [2]. ГПА — редкое заболевание, его распространённость в популяции составляет 25–60 на 1 млн человек, заболеваемость — 3–12 на 1 млн. Пик заболеваемости приходится на четвертое и пятое десятилетия, мужчины и женщины болеют с одинаковой частотой.
Несмотря на то, что клинико-рентгенологические проявления ГПА достаточно широко освещены в публикациях, при диагностике данного заболевания возникает немало трудностей, что связано с отсутствием у врачей настороженности в отношении развития данного заболевания. Для ГПА свойственна триада поражения органов с вовлечением верхних дыхательных путей (ВДП), легких и почек [2,4,5]. У подавляющего большинства больных (более 90%), развивается некротизирующее гранулематозное воспаление ВДП: язвенно-некротический ринит, синусит, поражение органа слуха, вовлечение трахеи и гортани с формированием подскладочной гранулемы. Возможна перфорация носовой перегородки с формированием седловидной деформации носа, развитие тяжёлого деструктивного пансинусита с распространением гранулематозной ткани в орбиту, потерей слуха, стенозом гортани.
Поражение лёгких (50–70%) характеризуется некротизирующим гранулематозным воспалением, которое при рентгенографическом исследовании определяется в виде узлов или инфильтратов, склонных к распаду и формированию полостей. Беспокоит кашель, иногда надсадный, боль в грудной клетке, кровохарканье, одышка, в каждом пятом случае поражение лёгких протекает бессимптомно, со скудной аускультативной картиной даже при тяжёлом поражении. При компьютерной томографии органов грудной клетки (КТ ОГК) отмечается также венчик вокруг очагов инфильтрации, связанный с перифокальным кровоизлиянием, изменения трахеобронхиального дерева в виде утолщения стенки и стеноза (в 15–25% случаев) и выпот в плевральную полость [2].
Поражение почек отмечается у 80% пациентов. Развиваются симптомы и признаки гломерулонефрита. Часто присутствуют изменения мочевого осадка и быстрое повышение уровня сывороточного креатинина. В результате могут возникать отёки и гипертензия, угрожающий жизни быстропрогрессирующий гломерулонефрит [2].
Для ГПА разработаны классификационные критерии, принятые Американской коллегией ревматологов в 1990 г. [6]. Всего предложено 4 критерия: воспаление носа или полости рта, развитие болезненных или безболезненных язв полости рта, гнойные или геморрагические выделения из носа, патологические изменения в лёгких, выявленные при рентгенологическом обследовании, наличие плотных инфильтратов или полостей, изменение мочевого осадка — макрогематурия (>5 эритроцитов в поле зрения) или скопление эритроцитов, гранулематозное воспаление при биопсии органов и тканей, гранулематозное воспаление в стенке артерий или артериол и образование гранулем в периваскулярных/экстраваскулярных областях.
Наличие двух и более критериев позволяет поставить диагноз с чувствительностью 88% и специфичностью 92 %.
План обследования при ГПА включает следующее:
- общий анализ крови (нормохромная анемия, тромбоцитоз, увеличение СОЭ);
- общий анализ мочи (микрогематурия, протеинурия);
- биохимический анализ крови (повышается содержание γ-глобулина, серомукоида, фибриногена, гаптоглобина, С-реактивный белок (СРБ), при поражении почек увеличивается уровень креатинина, мочевины);
- КТ грудной клетки и придаточных пазух носа;
- тесты на выявление АНЦА (антител к протеиназе-3 или миелопероксидазе);
- биопсия почек, слизистой полости носа.
Лечение включает в себя три основных этапа: индукция ремиссии (подавление активности заболевания), поддержание ремиссии, лечение рецидивов.
Для индукции ремиссии при поражении жизненно важных органов назначаются глюкокортикоиды (ГК) в сочетании с циклофосфамидом (вводится внутривенно) или генно-инженерный биологический анти-В-клеточный препарат ритуксимаб [7]. Лечение циклофосфамидом может продолжаться от 3 до 12 месяцев. Ритуксимаб назначают при непрерывно рецидивирующем течении васкулита, при неэффективности циклофосфамида или противопоказаниях к его применению. ГК сначала применяют внутривенно в виде пульс-терапии. Она предполагает введение высоких доз метилпреднизолона (0,5–1 мг/кг массы тела) в течение трёх дней. После этого переходят на таблетированную форму препарата. Для индукции ремиссии у больных без поражения жизненно важных органов может использоваться метотрексат (при отсутствии поражения почек) в дозе 20–25 мг в неделю и мофетила микофенолат в дозе 1–2 г в день в сочетании с таблетированными ГК. При тяжёлом поражении почек для сохранения их функции в дальнейшем может быть применён плазмаферез. В случае необходимости трансплантация почки проводится в период ремиссии при низком титре АНЦА. В дальнейшем этим больным назначают циклоспорин А и микофенолат мофетил.
Для поддержания ремиссии используются низкие дозы ГК в сочетании с одним из препаратов: азатиоприном, ритуксимабом, микофенолата мофетилом, метотрексатом. После достижения полной клинико-лабораторной ремиссии длительность противорецидивного лечения должна составлять не менее 24 месяцев.
Также обсуждается вопрос назначения триметоприма/сульфометаксозола [8]. Считается, что инфекционное поражение ВДП в дебюте ГПА является показанием к его назначению. Рекомендуется использовать по 2–3 таблетки 3 раза в день с оценкой эффекта через 6–8 недель. Описаны случаи использования препарата до 12 лет.
ГПА — это хроническое заболевание, поэтому на протяжении болезни могут наблюдаться периоды с различной выраженностью клинических проявлений. Прогноз зависит от локализации поражений. Если вовлечены только ВДП, то прогноз благоприятный. При поражении лёгких и почек прогноз зависит от своевременности назначения терапии и строгого соблюдения врачебных рекомендаций. Без лечения 80% случаев в течение года могут закончиться смертью. Однако сегодня большинству пациентов с ранним началом лечения удаётся достичь длительной ремиссии болезни. В приведённом ниже клиническом случае у пациента отмечается классическая триада симптомов (поражение верхних дыхательных путей, лёгких, почек), диагноз подтверждён морфологически при биопсии почки, слизистой полости носа.
Клинический случай
Пациент А., 34 лет, поступил в пульмонологическое отделение ГУЗ «Областная клиническая больница (ОКБ)», г. Саратова в феврале 2023 г. с направительным диагнозом «Пневмония». При поступлении отмечал приступообразный сухой кашель, ежедневное повышение температуры тела до 37,5–38,5°C в течение двух месяцев, снижение аппетита.
Из анамнеза известно, что с марта 2022 г. стал отмечать снижение слуха правого уха. С октября 2022 г. появился незначительный сухой кашель. Ежегодные флюорографические исследования были без патологии. С начала декабря 2022 г. наблюдалось ежедневное повышение температуры тела до фебрильных цифр, усиление интенсивности сухого кашля. Лечился самостоятельно жаропонижающими, антибактериальными препаратами без эффекта. Впоследствии присоединились летучие миалгии (боль в мышцах голеней, верхних конечностей), кашель приобрел интенсивный надсадный характер, периодически до рвоты, сопровождался отхождением пенистой белой мокроты. Амбулаторно выставлен диагноз «Острая респираторная вирусная инфекция», проводилась неспецифическая терапия (без эффекта). В связи с появлением боли в левом подреберье обратился к гастроэнтерологу, направлен на рентгенографию и КТ ОГК. При обследовании, со слов больного, выявлены признаки двусторонней пневмонии, в связи с чем 12 января 2023 г. госпитализирован в Саратовскую областную инфекционную больницу им. Н.Р. Иванова с диагнозом «Внебольничная двусторонняя полисегментарная пневмония, среднетяжёлое течение». Пациенту выполнены исследования на covid-19 и грипп (отрицательные результаты), кровь на маркеры вирусных гепатитов и ВИЧ (отрицательные результаты), малярию (отрицательный результат). Осмотрен фтизиатром: убедительных данных о туберкулёзе лёгких нет. Осмотрен оториноларингологом: правосторонний экссудативный отит, хронический атрофический ринит. При бронхоскопии выявлен диффузный эндобронхит. При КТ ОГК (30.01.2023 г.): множественные перибронховаскулярные крупные очаги, солидные с неровными нечеткими контурами и по типу матового стекла, разнокалиберные фокусы консолидации с неровными нечеткими контурами, медиастенальные и аксиллярные лимфатические узлы не увеличены (рис. 1).
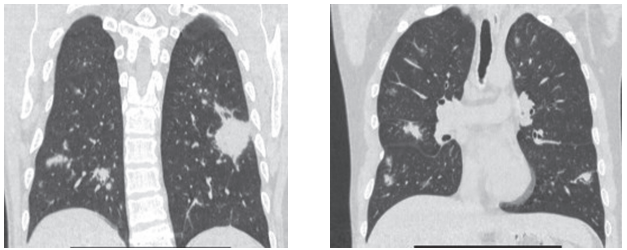
Рисунок 1. КТ органов грудной клетки от 30.01.2023 г. По всем сегментам обоих легких определяются множественные перибронховаскулярные крупные очаги, солидные с неровными нечеткими контурами и по типу матового стекла, разнокалиберные фокусы консолидации с неровными нечёткими контурами
При КТ брюшной полости обнаружена гепатоспленомегалия, признаки портальной гипертензии. В общем анализе крови (18.01.2023 г.) обращал на себя внимание тромбоцитоз (469×109/л). В динамике (29.01.2023 г.) число тромбоцитов увеличилось до 559×109/л, отмечено снижение уровня гемоглобина с 125 г/л до 111 г/л, нарастание эозинофилии — с 3% до 5%, СОЭ — с 5 мм/ч до 30 мм/ч. В общем анализе мочи и пробе Нечипоренко отмечалась гематурия (28–30 эритроцитов в поле зрения, 27250 эритроцитов в 1 мл). Также обращало на себя внимание повышение СРБ до 74,6–109,5 мг/л, при нормальном уровне прокальцитонина (менее 0,5 нг/мл).
В стационаре проводилась антибактериальная терапия (левофлоксацин 1000 мг в сутки в/в 12 дней, имипинем 3,0 г/сутки в/в кап в сочетании с кларитромицином 500 мг в сутки перорально 7 дней), противогрибковая терапия (флюконазол 150 мг в сути перорально, каспофунгин 50 мг в/в кап 1 раз в сутки). На фоне лечения сохранялся интенсивный сухой кашель, повышение температуры тела до 37,5°C ежедневно, при контрольной КТ ОГК — без динамики. 2 февраля 2023 г. пациент был переведён в пульмонологическое отделение ГУЗ «ОКБ» г. Саратова.
Из анамнеза жизни: бывший курильщик (индекс курения — 7 пачка/лет). Профессиональный, бытовой анамнез — без особенностей.
При поступлении состояние больного расценивалось как относительно удовлетворительное. Частота дыхания — 18 уд./мин. Аускультативно над лёгкими дыхание жёсткое, вдох равен выдоху, хрипов нет. SpO2 — 97% без оксигенотерапии. Тоны сердца ритмичные, частота сердечных сокращений — 70 уд./мин., АД — 120/80 мм рт. ст. Выявлялось увеличение шейных лимфатических узлов. Остальные органы — без особенностей.
При лабораторном обследовании сохранялось повышение СОЭ до 38 мм/час, снижение уровня гемоглобина (109 г/л), тромбоцитоз — до 800×109/л, эозинофилы — менее 1%, суточная протеинурия — 1,0 г/л, гематурия — 20500 (в пробе Нечипоренко), повышение СРБ — до 145,9 мг/мл, ферритин — 511 мкг/л, уровень прокальцитонина — в пределах нормы. При ультразвуковом исследовании органов брюшной полости подтверждено наличие гепатомегалии.
Учитывая характер поражения лёгочной ткани, отсутствие эффекта от антибактериальной терапии, выраженное повышение уровней СРБ, ферритина, нормальный прокальцитонин, изменения в общем анализе крови и мочи, было высказано предположение о наличии у пациента системного васкулита. Также не исключалось наличие лимфопролиферативного заболевания. В связи с чем проведено дообследование: уровень Ig E — 61 МЕ/мл3, антитела к антигенам цитоплазмы нейтрофилов, скрининг (ANCA-Screen) положительный, антитела (JgG) к dsДНК — 17,8 МЕ/мл, волчаночный антикоагулянт — отрицательный. При дополнительном сборе анамнеза удалось выяснить, что в течение нескольких лет отмечает отхождение сукровичного отделяемого из полости носа, появление корочек в носу. Осмотрен ЛОР-врачом повторно, выявлен правосторонний острый тубоотит, хронический атрофический ринит. Согласно результатам биопсии слизистой полости носа, обнаружены умеренный фиброз, выраженное продуктивное воспаление с наличием гигантских многоядерных клеток и клеток типа Пирогова-Лангханса, единичные гранулемы с явлениями фиброзирования, мелкими очагами некроза. При УЗИ периферических лимфатических узлов выявлено увеличение шейных лимфатических узлов. Выполнена пункционная биопсия шейного лимфоузла слева: найдены элементы лимфоидной ткани с явлениями гиперплазии. В связи с протеинурией, эритроцитурией выполнена нефробиопсия левой почки, по результатам которой выявлен фокальный некротизирующий и склерозирующий малоиммунный гломерулонефрит с 33% полулуний фиброзных и сопутствующим интерстициальным нефритом, острый канальцевый некроз. Данная морфологическая картина наиболее характерна для поражения почек при АНЦА-ассоциированном васкулите.
В связи с сохраняющейся фебрильной лихорадкой и отсутствием убедительных данных о бактериальной и вирусной инфекции были назначены системные ГК (преднизолон 30 мг в сутки перорально) с положительным эффектом в виде снижения температуры тела до субфебрильной, уменьшение выраженности кашля. С учётом поражения лёгких, верхних дыхательных путей, почек, молодого возраста, отсутствия эффекта от проводимой ранее антибактериальной терапии, противогрибковой терапии, положительного эффекта в виде снижения температуры тела до субфебрильной на фоне приема системных ГК, снижения острофазовых показателей (СРБ со 145,7 до 11,9 мг/мл, СОЭ с 38 до 20 мм/ч.) на фоне приёма системных ГК, положительного результата АНЦА, данных биопсии слизистой полости носа и почек был выставлен диагноз «Гранулематоз с полиангиитом, ассоциированный с АНЦА, с поражением лёгких, верхних дыхательных путей (правосторонний отит, атрофический ринит, гайморит в анамнезе), почек (нефрит). Тромбоцитоз, миалгии в анамнезе». Для дальнейшего лечения пациент был переведён в ревматологическое отделении ГУЗ «ОКБ». Продолжен приём преднизолона внутрь в дозе 30 мг в сутки с постепенным снижением дозы до 20 мг в сутки.
С учётом высокой активности заболевания, поражения лёгких, почек инициирована программная терапия циклофосфамидом, которая проводится с марта 2023 г. ежемесячно в дозе 1000 мг на введение. На этом фоне отмечалась положительная динамика: стойко нормализовалась температура, значительно уменьшилось отхождение кровянистых корочек из носа, купировался кашель, нормализовался уровень тромбоцитов, СРБ. Регистрировалось снижение протеинурии (с 3 г/сут. до 0,88 г/сут.), отсутствие гематурии. При повторной КТ лёгких от июня 2023 г. определяется выраженная положительная динамика за счёт значительного уменьшения в обоих лёгких размеров и количества участков уплотнения лёгочной ткани по типу «матового стекла» и консолидации (в настоящий момент выявляются единичные, преимущественно слева, размерами до 5–10 мм) (рис. 2).
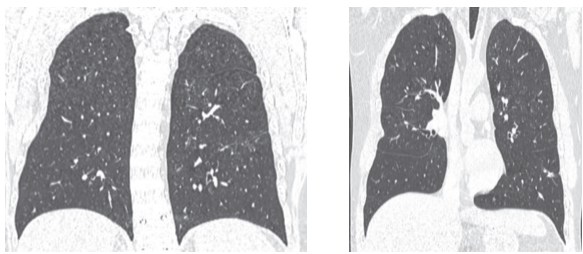
Рисунок 2. КТ органов грудной клетки от 16.06.2023 г. В динамике в обоих лёгких отмечается значительное уменьшение размеров и количества участков уплотнения легочной ткани по типу матового стекла и консолидации.
Программная терапия продолжается, состояние пациента удовлетворительное, доза преднизолона снижена до 10 мг в сутки. Также пациенту с самого начала с учётом поражения ВДП был назначен ко-тримаксозол.
Представленное клиническое наблюдение демонстрирует развитие генерализованного системного васкулита с поражением верхних дыхательных путей, лёгких, почек. Начало заболевания характеризовалось неспецифичностью клинической картины, что послужило причиной сложности диагностики. Важное значение в подтверждении диагноза имело как морфологическое исследование почки и слизистой оболочки носа, так и определение АНЦА. Поражение жизненно важных органов потребовало проведения терапии глюкокортикоидами и цитостатиками. Своевременное начало иммуносупрессивной терапии позволило через три месяца достигнуть снижения активности васкулита.
Данное клиническое наблюдение демонстрирует применение мультидисциплинарного подхода в диагностике ГПА с участием пульмонолога, ревматолога, нефролога, оториноларинголога, что имеет большое значение для ранней диагностики заболевания.
В наблюдениях середины прошлого века средняя продолжительность жизни после установления диагноза у нелеченых пациентов с АНЦА-ассоциированным васкулитом составляла 5 месяцев. За последние 40 лет выживаемость пациентов значимо улучшилась и при адекватном лечении может быть сопоставима с показателями общей популяции1 [2]. Таким образом, ранняя диагностика, своевременное начало терапии ГПА имеет важное значение для улучшения прогноза пациентов.
Заключение
В данном клиническом наблюдении продемонстрированы сложности своевременной верификации диагноза ГПА, что связано с отсутствием у врачей терапевтического профиля настороженности в отношении развития этого заболевания. Особенностью данного клинического случая является редкая распространённость представленной патологии, сложность в постановке диагноза в связи с полиорганностью поражения, отсутствие специфических признаков в дебюте заболевания, что потребовало проведения дифференциального диагноза. Раннее определение АНЦА повышает частоту диагностики ГПА, а своевременное установление диагноза позволяет как можно раньше назначить терапию и избежать инвалидизации пациентов.
1. Клинические рекомендации. Поражение почек при АНЦА-ассоциированных васкулитах (АНЦА-ассоциированный гломерулонефрит), 2021. – 88с. https://rusnephrology.org/wp-content/uploads/2021/02/ANCA.pdf
Список литературы
1. Wegener F. Uber eine eigenartige rhinogene granulomatose mit besonderer beteiligung des arteriensystems und der nieveu. Beitr. Pathol. 1939;102:36-68.
2. Анаев Э.Х., Баранова И.А., Белевский А.С. Легочные васкулиты: диагностика и лечение. Тер. Арх. 2018;(3):99-106. DOI: 10.26442/terarkh201890399-106.
3. Zhou P, Ma J, Wang G. Impact of interstitial lung disease on mortality in ANCA-associated vasculitis: A systematic literature review and meta-analysis. Chron Respir Dis. 2021;18:1479973121994562. DOI: 10.1177/1479973121994562
4. Клименко С., Кривошеев О. Гранулематоз Вегенера на современном этапе: варианты течения, прогноз. Врач. 2005;12:39-41. eLIBRARY ID: 14306935; EDN: MBCBBH
5. Синенко А.А., Кулаков Ю.В., Абрамочкина Е.Б., Лупач Н.М., Сюсина О.И., Файзенгер Е.М., и др. Опыт ведения больного с гранулематозом Вегенера: трудности диагностики и лечения. Вестник современной клинической медицины. 2011;4(2):46a-51. eLIBRARY ID: 16404054; EDN: NUZFNN
6. Leavitt RY, Fauci AS, Bloch DA, Michel BA, Hunder GG, Arend WP, et al. The American College of Rheumatology 1990 criteria for the classification of Wegener's granulomatosis. Arthritis Rheum. 1990;33(8):1101-7. DOI: 10.1002/art.1780330807
7. Бекетова ТВ. Международные рекомендации по лечению АНЦА-ассоциированных системных васкулитов. Современная ревматология. 2019;13(1):19–25. doi: 10.14412/1996-7012-2019-1-19-25.
8. Stegeman CA, Tervaert JW, de Jong PE, Kallenberg CG. Trimethoprim-sulfamethoxazole (co-trimoxazole) for the prevention of relapses of Wegener's granulomatosis. Dutch Co-Trimoxazole Wegener Study Group. N Engl J Med. 1996;335(1):16-20. DOI: 10.1056/NEJM199607043350103
Об авторах
Ю. Р. БарановаРоссия
Баранова Юлия Рашитовна - врач-пульмонолог пульмонологического отделения.
Саратов
И. А. Романова
Россия
Романова Ирина Александровна - к.м.н., доцент кафедры госпитальной терапии лечебного факультета.
Саратов
Р. Н. Стешенко
Россия
Стешенко Руслан Николаевич - к.м.н., заведующий пульмонологическим отделением.
Саратов
И. Ф. Мелехина
Россия
Мелехина Ирина Федоровна - заведующая ревматологическим отделением.
Саратов
Н. М. Никитина
Россия
Никитина Наталья Михайловна - д.м.н., заведующая кафедрой госпитальной терапии лечебного факультета.
Саратов
Тел.: +78452491437
Н. А. Кароли
Россия
Кароли Нина Анатольевна - д.м.н., профессор кафедры госпитальной терапии лечебного факультета.
Саратов
Рецензия
Для цитирования:
Баранова Ю.Р., Романова И.А., Стешенко Р.Н., Мелехина И.Ф., Никитина Н.М., Кароли Н.А. Гранулематоз Вегенера: трудности диагностики и лечения. Южно-Российский журнал терапевтической практики. 2023;4(4):95-100. https://doi.org/10.21886/2712-8156-2023-4-4-95-100
For citation:
Baranova Y.R., Romanova I.A., Steshenko R.N., Melehina I.F., Nikitina N.N., Karoli N.A. Wegener's granulomatosis: difficulties in diagnosis and treatment. South Russian Journal of Therapeutic Practice. 2023;4(4):95-100. (In Russ.) https://doi.org/10.21886/2712-8156-2023-4-4-95-100


























