Перейти к:
Влияние уровня липопротеида (а) на долгосрочные исходы у пациентов с острым коронарным синдромом и однососудистым поражением коронарных артерий
https://doi.org/10.21886/2712-8156-2024-5-3-46-53
Аннотация
Цель: оценить влияние уровней липопротеида (а) [Лп(а)] на долгосрочные исходы у пациентов с острым коронарным синдромом (ОКС) и однососудистым поражением коронарных артерий. Материалы и методы: в исследование были включены 110 пациентов с ОКС и однососудистым поражением коронарных артерий. Пациенты были разделены на две группы в зависимости от уровня Лп(а): Лп(а) > 50 мг/дл (n=22) и Лп(а) < 50 мг/дл (n=88). Основные исходы включали выживаемость и частоту повторных сердечно-сосудистых событий через 6, 12 и 36 месяцев. Статистический анализ включал t-тест, критерий хи-квадрат, метод Каплана-Мейера и многофакторную регрессию Кокса. Результаты: через 36 месяцев у пациентов с высоким уровнем Лп(а) была значительно выше частота повторных инфарктов миокарда (50% против 34.1%, p < 0.001) и смертность от всех причин (59.1% против 23.9%, p < 0.001) по сравнению с пациентами с нормальным уровнем Лп(а). Заключение: высокий уровень Лп(а) является значимым прогностическим фактором ухудшения долгосрочных исходов у пациентов с ОКС и однососудистым поражением коронарных артерий. Измерение уровня Лп(а) может способствовать улучшению стратегии ведения таких пациентов
Ключевые слова
Для цитирования:
Намитоков А.М., Кручинова С.В., Гендугова М.Н., Градовская М.В., Гилевич И.В. Влияние уровня липопротеида (а) на долгосрочные исходы у пациентов с острым коронарным синдромом и однососудистым поражением коронарных артерий. Южно-Российский журнал терапевтической практики. 2024;5(3):46-53. https://doi.org/10.21886/2712-8156-2024-5-3-46-53
For citation:
Namitokov A.M., Kruchinova S.V., Gendugova M.N., Gradovskaya M.V., Gilevich I.V. The impact of lipoprotein (a) levels on long-term outcomes in patients with acute coronary syndrome and single-vessel coronary artery disease. South Russian Journal of Therapeutic Practice. 2024;5(3):46-53. (In Russ.) https://doi.org/10.21886/2712-8156-2024-5-3-46-53
Введение
Атеросклероз коронарных артерий представляет собой сложное, полиэтиологическое заболевание, лежащее в основе значительной доли сердечно-сосудистой заболеваемости и смертности во всём мире. Этот патологический процесс характеризуется накоплением липидов, воспалительных клеток и соединительной ткани в стенке артерий, что приводит к их утолщению, потере эластичности и образованию атеросклеротических бляшек [1][2]. Сужение просвета артерий, обусловленное атеросклеротическими изменениями, ограничивает кровоток к миокарду, что вызывает клинические проявления, такие как стенокардия и острый коронарный синдром (ОКС).
Липопротеид (а) [Лп(а)] представляет собой уникальный класс липопротеинов, включающий аполипопротеин(a), который ковалентно связан с аполипопротеином B-100 [3]. Структурное сходство Лп(а) с плазминогеном позволяет ему конкурировать связывание с фибрином и ингибировать фибринолиз, что, вероятно, способствует развитию артериальных тромбозов [4]. Повышенные уровни Лп(а) связаны с повышенным риском атеросклеротических сердечно-сосудистых заболеваний, включая инфаркт миокарда и инсульт, а также раннего развития кальциноза и стенозирования аортального клапана [5].
Несмотря на признанную роль Лп(а) как независимого фактора риска сердечно-сосудистых заболеваний, его вклад в долгосрочные исходы после ОКС остается недостаточно изученным. Исследования показывают, что Лп(а) может способствовать прогрессированию атеросклероза и нестабильности бляшек, что увеличивает вероятность повторных коронарных событий [6].
Многочисленные исследования подтвердили роль Лп(а) как важного предиктора сердечно-сосудистых заболеваний. Например, работа [3] показала, что концентрации Лп(а) выше 50 мг/дл существенно увеличивают риск развития коронарного атеросклероза и связанных с ним осложнений. Более того, исследования Erqou et al. [7] подтвердили, что высокие уровни Лп(а) коррелируют с повышенным риском коронарных событий, инсульта и общей смертности.
В дополнение к этому исследование Caplice et al. [4] выявило, что Лп(а) связывается с сосудистым матриксом через аполипопротеин(a), что способствует отложению фибрина и ингибирует активацию плазминогена. Эти механизмы могут объяснять, почему пациенты с высокими уровнями Лп(а) имеют больший риск тромботических осложнений и худшие долгосрочные исходы после ОКС.
В настоящее время в мире активно изучается влияние Лп(а) на прогноз пациентов с коронарной болезнью сердца в различных клинических ситуациях. Одной из таких когорт являются пациенты с изолированным однососудистым поражением коронарных артерий, попавших в поле зрение кардиологов по поводу острого коронарного синдрома.
Цель исследования — оценка влияния уровней Лп(а) на отдалённые исходы у пациентов с ОКС при однососудистом поражении коронарных артерий.
Мы предполагаем, что высокий уровень Лп(а) ассоциируется с ухудшением долгосрочных исходов, таких как выживаемость и частота повторных сердечно-сосудистых событий, через 36 месяцев после ОКС.
Для минимизации роли фактора прогрессирования атеросклероза при многососудистом поражении различных локализаций нами в расчёт были приняты только пациенты с изолированным однососудистым поражением коронарных артерий.
Актуальность исследования
Исследование долгосрочных исходов у пациентов с ОКС при различных уровнях Лп(а) имеет важное клиническое значение. Понимание того, как Лп(а) влияет на выживаемость и частоту повторных сердечно-сосудистых событий, может способствовать улучшению стратегии ведения пациентов с высоким риском, особенно в свете ожидаемого появления таргетных препаратов, влияющих на гиперлипопротеидемию (а).
Материал и методы
Исследование представляет собой когортное ретроспективное одноцетровое наблюдение, проведённое для оценки роли Лп(а) в долгосрочных исходах у пациентов с ОКС при однососудистом поражении коронарных артерий. Все участники были разделены на две группы в зависимости от уровня Лп(а): группа с Лп(а) > 50 мг/дл и группа с Лп(а) < 50 мг/дл.
В исследование были включены 120 пациентов с диагнозом «ОКС» и однососудистым поражением коронарных артерий. Все пациенты были отобраны по следующим критериям: возраст старше 18 лет, острый коронарный синдром при поступлении, выполненная коронароангиография со стентирование 1 сосуда без наличия атеросклеротического поражения других коронарных артерий. Всем пациентам за период госпитализации было выполнено общеклиническое и лабораторное обследование по стандарту оказания помощи при остром коронарном синдроме, а также определен уровень лп (а). Для оценки уровня Лп(а) использовались стандартные лабораторные методы.
Основные определяемые исходы исследования включали выживаемость и частоту повторных сердечно-сосудистых событий (повторный инфаркт миокарда, инсульт, рестеноз стента, повторная госпитализация) через 6, 12 и 36 месяцев. Исходы оценивались на основании телефонных созвонов с пациентами или их родственниками.
В окончательный анализ включались пациенты, с которыми удалось установить связь и оценить отдаленный исход через 36 месяцев. Также из исследования исключались пациенты, умершие не от сердечно-сосудистых причин. Таким образом в окончательный анализ вошли 110 пациентов. Пациенты были разделены на две группы в зависимости от уровня Лп(а): Лп(а) > 50 мг/дл (n=22) и Лп(а) < 50 мг/дл (n=88). Основные демографические и клинические характеристики групп представлены в таблице 1.
Таблица/ Table 1
Исходная демографическая характеристика
Baseline demographic characteristics
Пациенты с Лп(а) больше 50мг/дл (n=22) | Пациенты с Лп(а) меньше 50мг/дл (n=88) | p | |
Возраст, лет | 52.18 | 51.22 | N/a |
Отягощённый семейный анамнез | 4.5% | 7.9 % | N/a |
Мужской пол | 86 % | 86.3 % | N/a |
Артериальная гипертензия | 59 % | 62 % | N/a |
Сахарный диабет 2 типа | 13.6 % | 12.5 % | 0.892 |
ИМТ, кг/м² | 28.69 | 28.36 | 0.732 |
Курение | 50 % | 40.9% | 0.459 |
Фракция выброса левого желудочка, % | 46.59 | 46.56 | N/a |
Уровень общего холестерина, ммоль/л | 6.1 | 5.55 | 0.419 |
Уровень ХС-ЛПНП, ммоль/л | 2.91 | 2.90 | 0.948 |
Уровень триглицеридов, ммоль/л | 2.15 | 1.61 | 0.053 |
Примечание: N/a — not applicable (не применимо), ИМТ — индекс массы тела;
ХС-ЛПНП — холестерин липопротеидов низкой плотности.
Для сравнения демографических и клинических характеристик между группами использовался t-тест для независимых выборок (для количественных переменных) и критерий хи-квадрат (для категориальных переменных). Если предположение о нормальности распределения данных нарушалось, применялся критерий Манна-Уитни.
Для оценки выживаемости использовался метод Каплана-Мейера. Этот метод позволял построить кривые выживаемости для каждой группы. Для сравнения кривых выживаемости между группами применялся лог-ранговый тест.
Для оценки влияния уровня Лп(а) на долгосрочные исходы использовалась многофакторная регрессия Кокса. Эта модель позволяла учесть влияние нескольких переменных одновременно и оценить риск (относительные риски, hazard ratios) для различных исходов. В регрессионные модели включались такие переменные, как возраст, пол, наличие ХБП, артериальная гипертензия, сахарный диабет, курение и ИМТ.
Уровень статистической значимости был установлен на уровне p<0,05. Все анализы проводились с использованием программного обеспечения SPSS версии 25.0 и R.
Результаты
Основные результаты исследования представлены в таблице 2.
Таблица/Table 2
Отдалённые результаты ЧКВ через 6, 12 и 36 месяцев
Remote results of PCI at 6, 12 and 36 months
Параметр | Нормальный Лп(а) (n=88) | Высокий Лп(а) (n=22) | p-значение |
Повторный ИМ (6 месяцев) | 4 | 2 | 0.753 |
Тромбоз стента (6 месяцев) | 2 | 1 | 1.000 |
Рестеноз стента (6 месяцев) | 10 | 1 | 0.578 |
Инсульт (6 месяцев) | 2 | 1 | 1.000 |
Повторная госпитализация (6 месяцев) | 23 | 4 | 0.618 |
Смерть от всех причин (6 месяцев) | 5 | 1 | 0.881 |
Повторный ИМ (12 месяцев) | 10 | 4 | 0.617 |
Тромбоз стента (12 месяцев) | 3 | 2 | 0.567 |
Рестеноз стента (12 месяцев) | 14 | 2 | 0.636 |
Инсульт (12 месяцев) | 3 | 1 | 1.000 |
Повторная госпитализация (12 месяцев) | 30 | 4 | 0.235 |
Смерть от всех причин (12 месяцев) | 13 | 2 | 0.896 |
Повторный ИМ (36 месяцев) | 30 | 11 | < 0.001 |
Тромбоз стента (36 месяцев) | 3 | 2 | 0.567 |
Рестеноз стента (36 месяцев) | 14 | 2 | 0.636 |
Инсульт (36 месяцев) | 8 | 7 | 0.064 |
Повторная госпитализация (36 месяцев) | 61 | 11 | 0.329 |
Смерть от всех причин (36 месяцев) | 21 | 13 | < 0.001 |
Примечание: ЧКВ — чрескожное коронарное вмешательство, ИМ — инфаркт миокарда
Анализ данных показал, что через 6 и 12 месяцев не было статистически значимых различий в выживаемости и частоте повторных сердечно-сосудистых событий между группами с нормальным и высоким уровнем Лп(а).
Через 36 месяцев наблюдались значительные различия между группами:
- Повторный инфаркт миокарда через 36 месяцев. Частота реинфарктов была значительно выше в группе с высоким уровнем Лп(а) (50%, 11 из 22) по сравнению с группой с нормальным уровнем — 34.1% (30 из 88) (p < 0.001).
- Смерть от всех сердечно-сосудистых причин через 36 месяцев. В группе с нормальным уровнем Лп(а) был зафиксирован 21 случай смерти (23.9%), тогда как в группе с высоким уровнем Лп(а) — 13 случаев (59.1%) (p < 0.001).
Кривые Каплана-Мейера на рисунке 1 демонстрируют расхождение кривых выживаемости в группах в зависимости от уровня Лп(а):
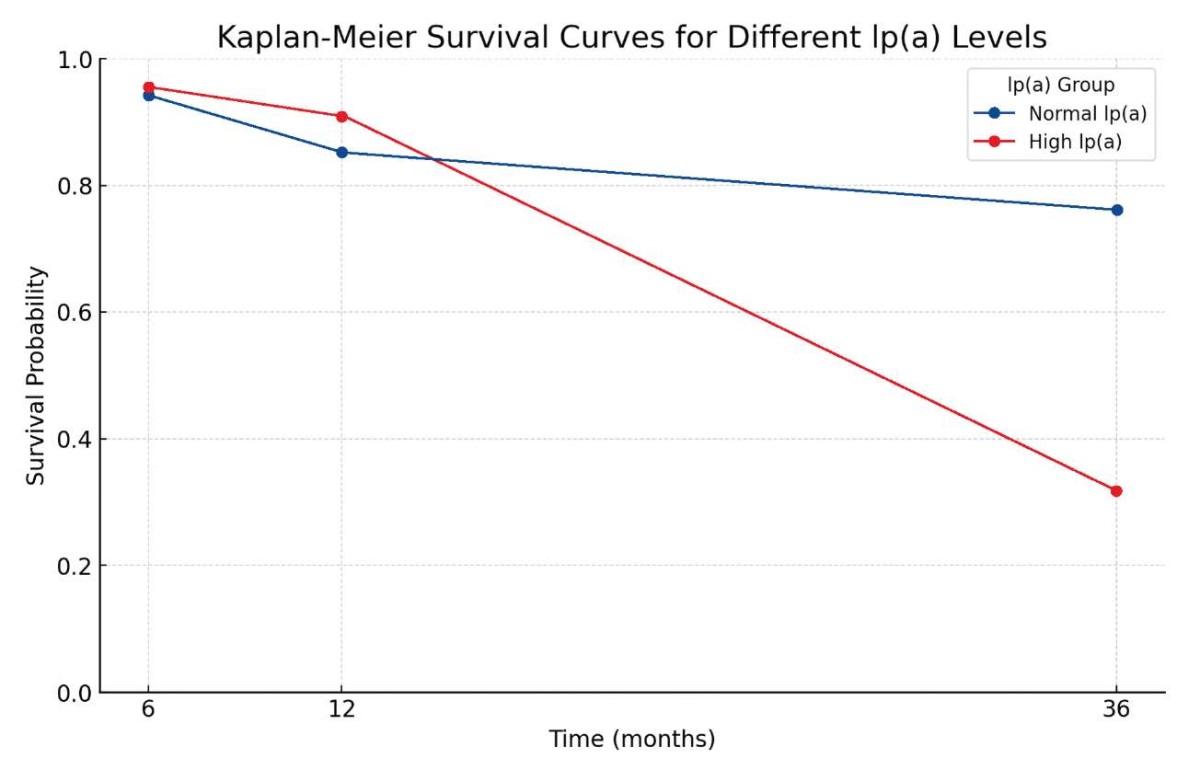
Рисунок 1. Различие в выживаемости в исследуемых группах
Figure 1. Difference in survival in the study groups
Модель логистической регрессии, включающая уровень Лп(а), возраст, пол, наличие хронической болезни почек (ХБП), артериальной гипертензии, сахарного диабета, курение и индекс массы тела (ИМТ), показала следующие результаты (табл. 3).
Таблица/Table 3
Модель логистической регрессии
Logistic Regression Model
Переменная | Коэффициент | Стандартная ошибка | Z-значение | P-значение |
Постоянная | -2.017 | 2.279 | -0.885 | 0.376 |
Лп(а), мг/дл | -0.024 | 0.007 | -3.459 | 0.001 |
Возраст, лет | 0.032 | 0.030 | 1.082 | 0.279 |
Пол | 0.605 | 0.721 | 0.839 | 0.401 |
ХБП, стадия | 0.298 | 0.841 | 0.354 | 0.723 |
Артериальная гипертензия | 0.575 | 0.505 | 1.138 | 0.255 |
Сахарный диабет | -0.471 | 0.713 | -0.661 | 0.509 |
Курение | 1.129 | 0.525 | 2.150 | 0.032 |
ИМТ, кг/м² | 0.019 | 0.052 | 0.372 | 0.710 |
Примечание: Лп(а) — липопротеид (а), ХБП — хроническая болезнь почек,
ИМТ — индекс массы тела.
Результаты модели показывают, что уровень Лп(а) и курение являются важными предикторами выживаемости через 36 месяцев у пациентов с острым коронарным синдромом при однососудистом поражении и ассоциируются с повышенным риском смертности. Псевдо R-квадрат модели составляет 0.1979, что указывает на то, что модель объясняет около 19.79% вариабельности в данных.
Значение AUC (площадь под кривой) равно 0.77, что указывает на достаточно хорошую предсказательную способность модели.
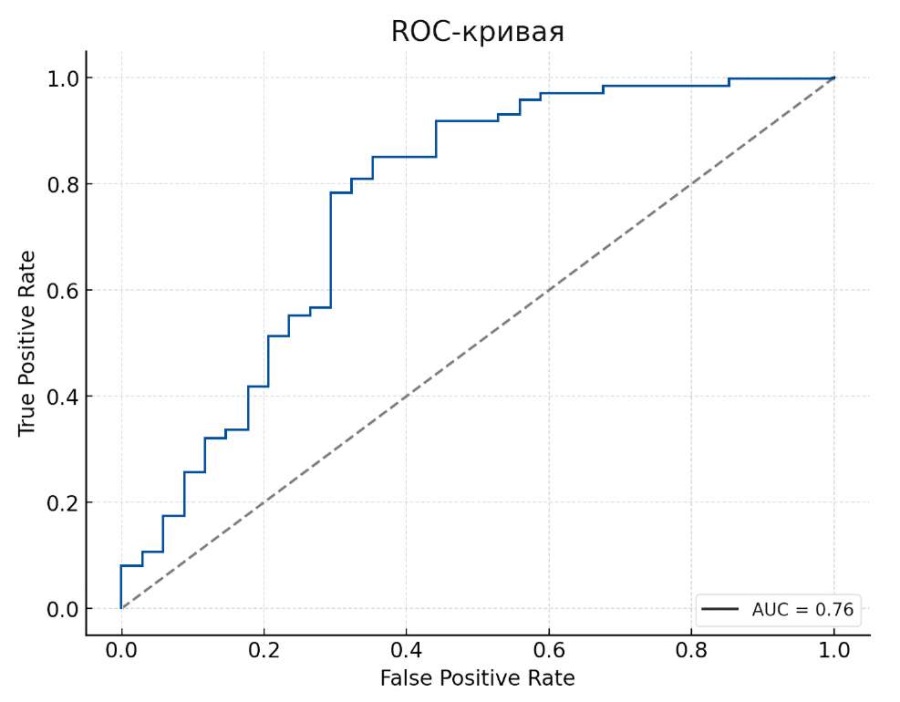
Рисунок 2. ROC-анализ
Figure 2. ROC analysis
Обсуждение
Результаты нашего исследования подтверждают значимость уровня Лп(а) как прогностического фактора долгосрочных исходов у пациентов с ОКС при однососудистом поражении коронарных артерий. Пациенты с высоким уровнем Лп(а) имели значительно худшие долгосрочные исходы, включая выживаемость, частоту повторных сосудистых катастроф и смертность через 3 года после ОКС.
На данный момент нет единого стандарта по определению Лп(а) у всех пациентов с ОКС [8]. Однако с учётом результатов нашего исследования и данных литературы [9] становится ясно, что измерение Лп(а) может быть важным шагом в оценке риска у пациентов с ОКС. Рекомендации Американского колледжа кардиологии (ACC) предполагают измерение Лп(а) у пациентов с подозрением на генетически обусловленные формы гиперхолестеринемии, а также у тех, у кого реакция на статины менее ожидаемая [10]. Исследования показывают, что у пациентов с высоким уровнем Лп(а), которые продолжают иметь высокий уровень Лп(а) даже при терапии статинами, риск сердечно-сосудистых событий остается высоким [11]. Мета-анализы подтверждают, что высокий уровень Лп(а) является сильным предиктором риска сердечно-сосудистых заболеваний, особенно у пациентов с уже имеющимися атеросклеротическими заболеваниями [7][12].
Неоднозначен и не до конца изучен вопрос столь патогенного влияния Лп(а) на атерогенез. В целом современная концепция предполагает, что Лп(а) способствует развитию атеросклероза и тромбоза через несколько механизмов:
- Интерференция с фибринолизом: Лп(а) структурно схож с плазминогеном и может ингибировать фибринолиз, что способствует тромбообразованию [13].
- Проинфламаторные свойства: Лп(а) усиливает воспаление в атеросклеротических бляшках, делая их более нестабильными [6].
- Окисленные фосфолипиды: Лп(а) может переносить окисленные фосфолипиды, что увеличивает воспаление и риск тромбоза [14].
Учитывая значительное влияние Лп(а) на долгосрочные исходы у пациентов с ОКС, важно рассмотреть более широкое применение тестирования на Лп(а) в клинической практике. Это особенно актуально для пациентов с неоднозначными исходами терапии статинами и тех, кто находится в зоне высокого риска сердечно-сосудистых событий.
Терапевтические подходы к коррекции Лп(а) сводятся к применению PCSK-9 таргетных агентов и аферезу. Применение PCSK9-таргетных агентов, таких как алирокумаб и инклисиран, показало снижение уровня Лп(а) и улучшение клинических исходов у пациентов с высоким уровнем Лп(а) [15-17].
Что касается афереза, то этот метод показал значительное снижение уровня Лп(а) и улучшение исходов у пациентов с высоким Лп(а), особенно в Германии [18].
Ещё один вопрос, логично возникающий из выводов нашего исследования. Что является более предпочтительным методом реваскуляризации миокарда при однососудистом поражении передней нисходящей артерии — чрескожное коронарное вмешательство или маммаро-коронарное шунтирование?
Ограничения и направления для будущих исследований:
- Размер выборки. Ограниченное количество пациентов, особенно в группе с высоким уровнем Лп(а), может влиять на статистическую мощность и обобщаемость результатов.
- Однососудистое поражение. Результаты исследования применимы только к пациентам с однососудистым поражением, что ограничивает возможность экстраполяции данных на пациентов с многососудистым поражением.
- Различные факторы риска. Влияние других факторов риска, таких как генетические и экологические факторы, требует дополнительного изучения.
Заключение
Наше исследование подчёркивает важность измерения уровня Лп(а) у пациентов с ОКС для прогнозирования долгосрочных исходов. Высокий уровень Лп(а) является независимым фактором риска, ассоциированным с повышенной смертностью и частотой повторных сердечно-сосудистых событий через 36 месяцев. Дальнейшие исследования с более крупными выборками и разнообразными популяциями необходимы для подтверждения этих выводов и разработки эффективных стратегий лечения.
Финансирование. Исследование проведено при поддержке Кубанского научного фонда в рамках научного проекта № МФИ-20.1/63.
Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов.
Список литературы
1. Ross R. Atherosclerosis--an inflammatory disease. N Engl J Med. 1999;340(2):115-126. DOI: 10.1056/NEJM199901143400207
2. Libby P, Hansson GK. Inflammation and immunity in diseases of the arterial tree: players and layers. Circ Res. 2015;116(2):307-311. DOI: 10.1161/CIRCRESAHA.116.301313
3. Nordestgaard BG, Chapman MJ, Ray K, Borén J, Andreotti F, Watts GF, et al. Lipoprotein(a) as a cardiovascular risk factor: current status. Eur Heart J. 2010;31(23):2844-2853. DOI: 10.1093/eurheartj/ehq386
4. Caplice NM, Panetta C, Peterson TE, Kleppe LS, Mueske CS, Kostner GM, et al. Lipoprotein (a) binds and inactivates tissue factor pathway inhibitor: a novel link between lipoproteins and thrombosis. Blood. 2001;98(10):2980-2987. DOI: 10.1182/blood.v98.10.2980
5. Kronenberg F, Mora S, Stroes ESG, Ference BA, Arsenault BJ, Berglund L, et al. Lipoprotein(a) in atherosclerotic cardiovascular disease and aortic stenosis: a European Atherosclerosis Society consensus statement. Eur Heart J. 2022;43(39):3925-3946. DOI: 10.1093/eurheartj/ehac361
6. Tsimikas S. A Test in Context: Lipoprotein(a): Diagnosis, Prognosis, Controversies, and Emerging Therapies. J Am Coll Cardiol. 2017;69(6):692-711. DOI: 10.1016/j.jacc.2016.11.042
7. Emerging Risk Factors Collaboration; Erqou S, Kaptoge S, Perry PL, Di Angelantonio E, Thompson A, et al. Lipoprotein(a) concentration and the risk of coronary heart disease, stroke, and nonvascular mortality. JAMA. 2009;302(4):412-423. DOI: 10.1001/jama.2009.1063
8. Афанасьева О.И., Ежов М.В., Покровский С.Н. Определение концентрации липопротеида(а) в клинической практике: актуальность и нерешенные вопросы. Атеросклероз и Дислипидемии. 2021;2(43):47-56. DOI: 10.34687/2219-8202.JAD.2021.02.0004.
9. Намитоков A.M., Зафираки В.К., Кручинова С.В., Ишевская О.П., Космачева Е.Д. Практическая значимость измерения уровня липопротеида(а) для стратификации риска. Атеросклероз и Дислипидемии. 2022;2(47):15-20. DOI: 10.34687/2219-8202.JAD.2022.02.0003
10. American College of Cardiology. An Update on Lipoprotein(a): The Latest on Testing, Treatment, and Guideline Recommendations. ACC; 2024.
11. Schwartz GG, Steg PG, Szarek M, Bittner VA, Diaz R, Goodman SG, et al. Peripheral Artery Disease and Venous Thromboembolic Events After Acute Coronary Syndrome: Role of Lipoprotein(a) and Modification by Alirocumab: Prespecified Analysis of the ODYSSEY OUTCOMES Randomized Clinical Trial. Circulation. 2020;141(20):1608-1617. DOI: 10.1161/CIRCULATIONAHA.120.046524
12. Wang G, Xia M, Liang C, Pu F, Liu S, Jia D. Prognostic value of elevated lipoprotein (a) in patients with acute coronary syndromes: a systematic review and meta-analysis. Front Cardiovasc Med. 2024;11:1362893. DOI: 10.3389/fcvm.2024.1362893
13. Miles LA, Fless GM, Levin EG, Scanu AM, Plow EF. A potential basis for the thrombotic risks associated with lipoprotein(a). Nature. 1989;339(6222):301-303. DOI: 10.1038/339301a0
14. Leibundgut G, Arai K, Orsoni A, Yin H, Scipione C, Miller ER, et al. Oxidized phospholipids are present on plasminogen, affect fibrinolysis, and increase following acute myocardial infarction. J Am Coll Cardiol. 2012;59(16):1426-1437. DOI: 10.1016/j.jacc.2011.12.033
15. Bittner VA, Szarek M, Aylward PE, Bhatt DL, Diaz R, Edelberg JM, et al. Effect of Alirocumab on Lipoprotein(a) and Cardiovascular Risk After Acute Coronary Syndrome. J Am Coll Cardiol. 2020;75(2):133-144. DOI: 10.1016/j.jacc.2019.10.057
16. Ray KK, Wright RS, Kallend D, Koenig W, Leiter LA, Raal FJ, et al. Two Phase 3 Trials of Inclisiran in Patients with Elevated LDL Cholesterol. N Engl J Med. 2020;382(16):1507-1519. DOI: 10.1056/NEJMoa1912387
17. Raal FJ, Kallend D, Ray KK, Turner T, Koenig W, Wright RS, et al. Inclisiran for the Treatment of Heterozygous Familial Hypercholesterolemia. N Engl J Med. 2020;382(16):1520-1530. DOI: 10.1056/NEJMoa1913805
18. Heigl F, Pflederer T, Klingel R, Hettich R, Lotz N, Reeg H, et al. Lipoprotein apheresis in Germany - Still more commonly indicated than implemented. How can patients in need access therapy? Atheroscler Suppl. 2019;40:23-29. DOI: 10.1016/j.atherosclerosissup.2019.08.038
Об авторах
А. М. НамитоковРоссия
Намитоков Алим Муратович, к.м.н., заведующий кардиологическим отделением №2 для больных с инфарктом миокарда; доцент кафедры терапии №1
Краснодар
С. В. Кручинова
Россия
Кручинова София Владимировна, к.м.н., врач-кардиолог кардиологического отделения №2 для больных с инфарктом миокарда; ассистент кафедры терапии No 1
Краснодар
М. Н. Гендугова
Россия
Гендугова Милана Нургалиевна, врач-кардиолог приемного отделения; аспирант кафедры терапии No 1
Краснодар
М. В. Градовская
Россия
Градовская Мария Викторовна, врач ультразвуковой диагностики
Краснодар
И. В. Гилевич
Россия
Гилевич Ирина Викторовна, к.м.н., заведующий лабораторией разработки и изучения новых технологий лечения заболеваний; ассистент кафедры онкологии с курсом торакальной хирургии ФПК и ППС
Краснодар
Рецензия
Для цитирования:
Намитоков А.М., Кручинова С.В., Гендугова М.Н., Градовская М.В., Гилевич И.В. Влияние уровня липопротеида (а) на долгосрочные исходы у пациентов с острым коронарным синдромом и однососудистым поражением коронарных артерий. Южно-Российский журнал терапевтической практики. 2024;5(3):46-53. https://doi.org/10.21886/2712-8156-2024-5-3-46-53
For citation:
Namitokov A.M., Kruchinova S.V., Gendugova M.N., Gradovskaya M.V., Gilevich I.V. The impact of lipoprotein (a) levels on long-term outcomes in patients with acute coronary syndrome and single-vessel coronary artery disease. South Russian Journal of Therapeutic Practice. 2024;5(3):46-53. (In Russ.) https://doi.org/10.21886/2712-8156-2024-5-3-46-53
JATS XML


























