Перейти к:
Клинический случай установления диагноза корригированной транспозиции магистральных сосудов у пациентки в зрелом возрасте
https://doi.org/10.21886/2712-8156-2025-6-1-81-87
Аннотация
В рамках публикации рассмотрен врождённый порок сердца — транспозиция магистральных сосудов, летальность при котором в первый месяц жизни составляет 50 %, в возрасте до года - 90 % случаев. Одним из вариантов транспозиции аорты и лёгочной артерии является корригированная транспозиция. В отечественной литературе описываются клинические случаи корригированной транспозиции магистральных сосудов в педиатрии, выявленные в первые месяцы и годы жизни ребенка. В статье представлен клинический случай корригированной транспозиции магистральных сосудов, впервые выявленной у пациентки в зрелом возрасте.
Ключевые слова
Для цитирования:
Гутова С.Р., Скибицкий В.В., Фендрикова А.В. Клинический случай установления диагноза корригированной транспозиции магистральных сосудов у пациентки в зрелом возрасте. Южно-Российский журнал терапевтической практики. 2025;6(1):81-87. https://doi.org/10.21886/2712-8156-2025-6-1-81-87
For citation:
Gutova S.R., Skibitsky V.V., Fendrikova A.V. A clinical case of diagnosis of the corrected transposition of the great arteries in an adult patient. South Russian Journal of Therapeutic Practice. 2025;6(1):81-87. (In Russ.) https://doi.org/10.21886/2712-8156-2025-6-1-81-87
Введение
Транспозиция магистральных сосудов (ТМС) — врождённый порок сердца (ВПС), относящийся к группе «синих» пороков. ТМС связана с аномалиями конотрункуса и характеризуется дискордантным желудочково-артериальным соединением, при котором лёгочный ствол отходит от морфологически левого желудочка (ЛЖ), а аорта (Ао) — от анатомически правого желудочка (ПЖ) [1][2]. Частота встречаемости ТМС составляет 2,5–5% среди всех ВПС, чаще выявляется у лиц мужского пола [2]. Связь ТМС с хромосомными аномалиями и генетическими дефектами в литературе не указывается [2]. Впервые порок был описан английским хирургом и патологом M. Baillie в 1797 г. [3]. Прижизненный диагноз транспозиции Ао и лёгочной артерии (ЛА) первыми поставили F. Fanconi (1932 г.) и H. Taussig (1938 г.) [4].
ТМС может быть как при нормальном (situs solitus, D-транспозиция), так и при обратном (situs inversus, L-транспозиция) расположении предсердий [2]. Для полной ТМС (D-транспозиция) характерно конкордантное предсердно-желудочковое и дискордантное желудочково-артериальное соединение [1][5][6]. Анатомически правое предсердие (ПП), в которое впадают полые вены соединяется с морфологически ПЖ, продолжением которого является Ао, несущая венозную кровь к тканям организма. Анатомически левое предсердие (ЛП) соединено с морфологически ЛЖ, от которого отходит ствол ЛА, несущий артериальную кровь к лёгким. При этом анатомически ПЖ находится справа от ЛЖ, как при нормально сформированном сердце. Буква D в данной ситуации означает расположение Ао относительно ЛА: в 80% случаях справа от нее, редко слева или спереди [6]. Таким образом, при D-ТМС круги кровообращения разделены. Кроме того, в малом круге кровообращения циркулирует артериальная кровь, а в большом — венозная, что несовместимо с жизнью.
Выживаемость в таких случаях зависит от сброса крови, который может происходить на уровне межжелудочковой перегородки (МЖП), межпредсердной перегородки (МПП) и магистральных сосудов [5]. При D-ТМС выделяют две категории больных. К первой относятся лица с отсутствием дефекта МЖП (ДМЖП) (так называемая простая ТМС) [2][5]. В этой ситуации смешивание крови большого и малого кругов кровообращения происходит через открытое овальное окно (ООО) или дефект МПП (ДМПП), обычно типа ostium secundum, а также на уровне магистральных артерий через открытый артериальный проток (ОАП) [2][5]. В данном случае совмещение крови незначительное, что и определяет выраженную гипоксемию. Состояние больных с полной простой ТМС без ДМЖП более тяжёлое, чем у лиц с ДМЖП, которое может усугубиться при закрытии ОАП. У больных с простой D-ТМС имеется тенденция к развитию лёгочной гипертензии в более раннем возрасте, в связи с чем хирургическая коррекция показана в первые 2–4 недели жизни [2].
Вторая категория представлена пациентами с ДМЖП (сложная ТМС) [2][5]. В данном случае объединение лёгочного и системного кровотока происходит и на уровне предсердий через ООО или ДМПП, обычно типа ostium secundum, и на этапе желудочков посредством ДМЖП, и на высоте магистральных сосудов через ОАП. Степень гипоксемии у больных с полной сложной ТМС зависит от размера дефектов и объёма смешивания артериальной и венозной крови. Больные с ДМЖП при рождении менее цианотичны, но уже к 3–4 месяцам жизни у них развивается лёгочная гипертензия и признаки правожелудочковой сердечной недостаточности. В связи с этим пациентам с полной сложной ТМС необходимо проводить хирургическую коррекцию порока в возрасте от 2 недель до 3 месяцев [2].
Оперативное вмешательство при D-ТМС заключается в артериальном переключении и коррекции сопутствующих пороков [2]. При простой ТМС в первые дни рекомендовано выполнение паллиативной операции, заключающейся в баллонной атриосептостомии по Rashkind [2]. При упущении подходящего момента выполнения артериального переключения проводят суживание ЛА с межартериальным шунтированием или без него, затем операцию Jatene [2].
Для врождённой корригированной ТМС (L-транспозиция) характерно дискордантное предсердно-желудочковое и желудочково-артериальное соединение [1][5][6]. Анатомически ПП соединено с морфологически ЛЖ, продолжением которого является ствол ЛА, несущий венозную кровь. ЛП, в которое впадают лёгочные вены, соединено с анатомически ПЖ, от которого отходит Ао, несущая артериальную кровь. Ао обычно находится спереди от ствола ЛА. Имеется фиброзный контакт задней створки клапана ЛА с передней створкой митрального клапана (МК) (в отдельных случаях наблюдается непрямой фиброзный контакт клапана ЛА с трёхстворчатым клапаном (ТК)). Как и при D-ТМС, выносящие тракты желудочков и магистральные артерии идут параллельно.
Корригированная ТМС без сопутствующих пороков встречается крайне редко [5]. В 90% случаев обнаруживаются изменения анатомически ТК, проявляющиеся в виде дисплазии (смещение септальной створки клапана к верхушке желудочка, напоминающее аномалию Эбштейна, прикрепление сухожильных хорд створок клапана напрямую к перегородке и трабекулам желудочка, недоразвитие отдельных групп папиллярных мышц) и сопровождающееся артериальной недостаточностью атриовентрикулярного (АВ) клапана, изредка стенозом [5][6]. В 70% случаях встречается ДМЖП (чаще всего перимембранозный), в 40% — подклапанный стеноз ЛА, в 10% — субаортальный стеноз и у большей части больных — коарктация Ао. При комбинации корригированной ТМС с ДМЖП отмечается высокая лёгочная гипертензия, а при добавлении и стеноза ЛА гемодинамика порока напоминает изменения, характерные для тетрады Фалло.
C точки зрения физиологии, при L-ТМС круги кровообращения функционируют правильно: кровь из лёгочных вен идет в Ао, а из полых — в легочный ствол. Однако роль системного желудочка выполняет морфологически ПЖ. Корригированная ТМС может протекать совершенно бессимптомно при отсутствии гемодинамически значимого внутрисердечного сброса крови, тяжёлой клапанной недостаточности и стенозов [6]. Несмотря на то, что сопутствующие нарушения почти всегда есть, многие больные долгое время ведут нормальный образ жизни. Основное прогностическое значение имеет функция ПЖ, выполняющего при этом пороке функцию ЛЖ, и трикуспидальная (артериальная) недостаточность.
Для пациентов с бессимптомной L-ТМС достаточно регулярного наблюдения и профилактики инфекционного эндокардита [6]. При сопутствующих пороках (ДМЖП и стеноз ЛА) тактика лечения та же, что при изолированных поражениях без ТМС. При тяжёлом подклапанном стенозе ЛА устраняют ДМЖП и создают шунт (кондуит) из морфологически ЛЖ в ЛА, а при тяжёлой трикуспидальной (артериальной) недостаточности проводят реконструктивную операцию или протезирование клапана [6].
Выявление ТМС у плода вызывает сложности. Внутриутробное кровообращение при этой аномалии не страдает. Диагностическим критерием порока является параллельный ход магистральных артерий (в норме перекрещивающихся), а также визуализация крупного сосуда (ЛА), который берёт начало от ЛЖ и делится на две ветви.
Описание клинического случая
Больная Э., 1988 г. р., 17.09.2019 г. обратилась в приёмное отделение государственного бюджетного учреждения здравоохранения Республики Адыгея «Майкопская городская клиническая больница» с жалобами на одышку при умеренной физической нагрузке, общую слабость, учащенное сердцебиение.
Анамнез заболевания: ухудшение состояния в течение последних двух месяцев. На учете у кардиолога и терапевта не состояла, медикаментозную терапию не получала.
Из анамнеза жизни: пациентка Э. родилась от первой беременности, роды в срок, единственная в семье. При рождении вес — 2900 гр., рост — 49 см. У больной имеется дочь от второй беременности. Ребенок здоров, без ВПС. От первой беременности ребенок родился мёртвым. ВПС у родственников первой степени родства пациентки при проведении эхокардиогрфии (ЭхоКГ) не выявлены.
Данные объективного обследования: состояние пациентки на момент осмотра средней степени тяжести. Больная правильного телосложения, правильного питания. Кожные покровы чистые, бледноватой окраски. Грудная клетка обычной формы, обе половины равномерно участвуют в акте дыхания. При перкуссии — лёгочный звук. В лёгких дыхание везикулярное, хрипов нет, частота дыхательных движений — 20 в минуту. Сатурация кислорода в крови — 96%. АД — 100/60 мм рт. ст. При аускультации сердца тоны приглушены, ритм правильный. Частота сердечных сокращений (ЧСС) — 100 ударов в минуту. Выслушивается систолический шум на верхушке. Пульсация на периферических артериях сохранена. Живот обычной формы, при пальпации мягкий, безболезненный. Печень не увеличена, не выступает из-под края рёберной дуги. Селезёнка не пальпируется. Периферических отёков нет.
Выполнены стандартные лабораторные исследования: клинический анализ крови и мочи, биохимический анализ крови в пределах нормативных значений.
По данным ЭКГ, синусовый ритм с ЧСС 90 в минуту. Электрическая ось сердца отклонена влево. Очаговые изменения миокарда передней стенки, верхушки и боковой стенки.
При проведении ЭхоКГ, представленной на рисунках 1–4, выявлено правосформированное леворасположенное сердце. Печень расположена в анатомически положенном месте (справа). Анатомически ПП (ориентир — заслонка полой вены) соединён с анатомически ЛЖ (анатомический ориентир — гладкая эндокардиальная поверхность), расположенным справа (дискордантное АВ-соединение). Диаметр ПП — 36×42 мм. Базальный диаметр ЛЖ из апикальной позиции (приточный отдел) — 38 мм, глобальная сократимость не снижена. Толщина боковой стенки ЛЖ — 7–8 мм. ПП соединяется с ЛЖ посредством двустворчатого (анатомически митрального) клапана, крепление створок которого расположено ниже крепления створок ТК. Митральная регургитация (+/++). От анатомически ЛЖ отходит ствол ЛА (несёт венозную кровь), с наличием митрально-легочного фиброзного продолжения. Диаметр ЛА на уровне клапана — 26 мм. Максимальный градиент на клапане ЛА — 8 мм рт. ст. Пульмональная регургитация (+). Визуализируются бифуркация и ветви ЛА, не расширены. Слева от ЛЖ располагается анатомически ПЖ (анатомический ориентир — модераторный пучок и трабекулярность). ПЖ соединяется с анатомически ЛП посредством анатомически ТК. Трикуспидальная регургитация (++/+++), створки утолщены. Сухожильные хорды ТК крепятся к перегородке и трабекулам ПЖ. Базальный диаметр ПЖ из апикальной позиции — 49 мм. Фракция изменения площади (ФИП) ПЖ — 40% (норма — более 35%) [7][8]. Систолическая экскурсия плоскости трикуспидального кольца в М-режиме (TAPSE) — 14,7 мм (норма — более 17 мм) [7][8]. Толщина боковой стенки ПЖ — 7–8 мм, МЖП — 9 мм. Диаметр ЛП — 46×68 мм. Объём ЛП — 80 мл. От анатомически ПЖ отходит Ао (несёт артериальную кровь). Диаметр корня Ао — 34 мм, восходящего отдела Ао — 29 мм, дуга Ао — 29 мм. Аортальный клапан (АК) двухстворчатый, регургитации нет. Максимальный градиент на АК — 8 мм рт. ст. Скорость кровотока в нисходящем отделе Ао в пределах нормы. Отсутствует контакт между артериальным (анатомически ТК) АВ-клапаном и магистральным сосудом (Ао), что свидетельствует об инверсионном положении сосудов. Ао расположена спереди и слева от ЛА. Патологические шунты через МПП и МЖП при цветовом картировании не регистрируются, смещения септальной створки ТК нет. Допплер: ЕТК — 108 см/сек., АТК — 32 см/сек., ебокТК — 19 см/сек., еМЖП — 11,7 см/сек., sТК — 8 см/сек. (норма для ТК — более 9,5 см/сек.) [7], что позволяет косвенно судить о наличии нарушения регионарной систолической функции ПЖ. ta-eТК — 625 мс, tsТК — 354 мс, Teim-индекс — 0,77 (норма — менее 0,54), что также косвенно указывает на наличие нарушения регионарной систолической функции ПЖ. Е/еТКср 7,5 — косвенный признак отсутствия высокого конечного диастолического давления в ПЖ [7][8].
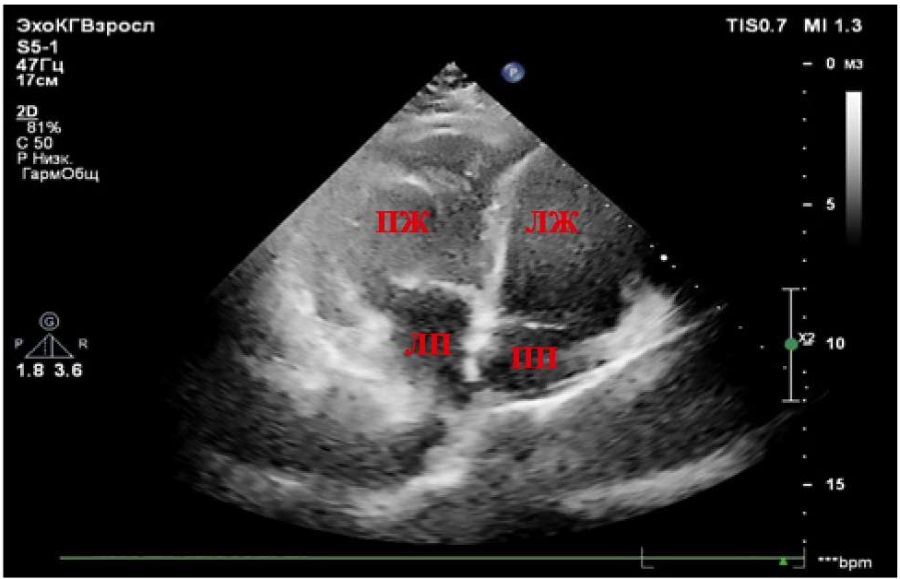
Рисунок 1. Апикальная четырёхкамерная позиция (инверсия желудочков). Анатомический ориентир — ПП (заслонка полой вены), ЛЖ (гладкая эндокардиальная поверхность), ПЖ (модераторный пучок и трабекулярность).
Примечание: ПЖ — правый желудочек, ЛЖ — левый желудочек, ЛП — левое предсердие, ПП — правое предсердие.
Figure 1. Apical four-chamber view (ventricular inversion). Anatomical landmarks: RA (caval valve), LV (smooth endocardial surface), RV (moderator bundle and trabecularity).
Note: RV — right ventricle, LV — left ventricle, LA — left atrium, RA — right atrium.

Рисунок 2. Апикальная четырёхкамерная позиция. Умеренная недостаточность артериального (анатомически трикуспидального клапана). Левое предсердие соединяется с правым желудочком посредством артериального (анатомически трикуспидального) клапана, крепление створок которого расположено выше крепления створок митрального клапана (анатомический ориентир).
Примечание: ТК — трикуспидальный клапан.
Figure 2. Apical four-chamber view. Moderate insufficiency of the arterial (anatomically tricuspid) valve. The left atrium communicates with the right ventricle via the arterial (anatomically tricuspid) valve, the attachment of the cusps of which is located above the attachment of the mitral valve cusps (anatomical landmark).
Note: TC — tricuspid valve.
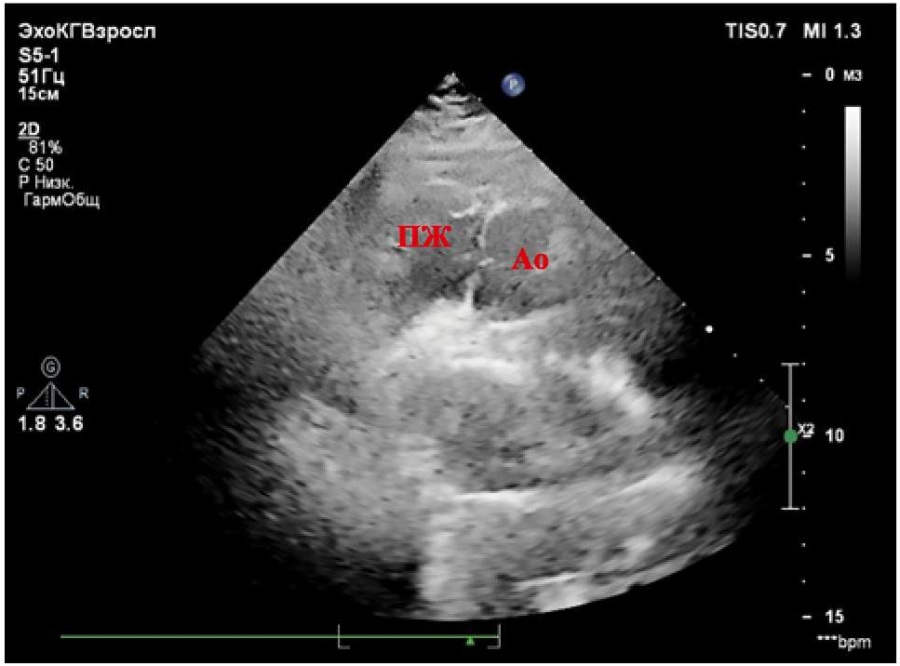
Рисунок 3. Парастернальная позиция по длинной оси. Отхождение аорты от анатомически правого желудочка. Отсутствует митрально-аортальное соединение.
Примечание: ПЖ — правый желудочек, Ао — аорта.
Figure 3. Parasternal long axis view. Aorta originates from the anatomically right ventricle. There is no mitral-aortic junction.
Note: RV — right ventricle, Ao — aorta.
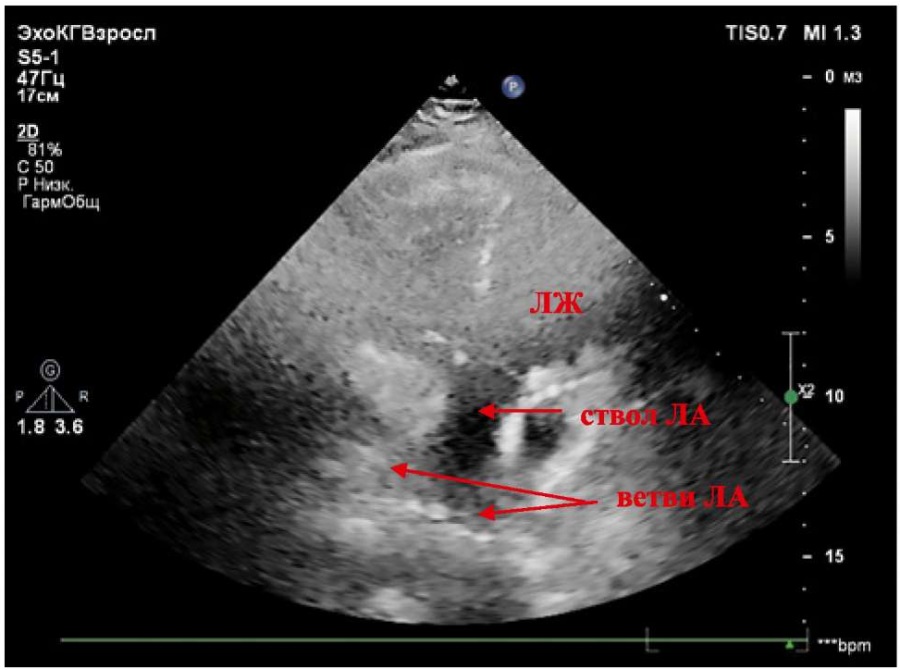
Рисунок 4. Апикальная пятикамерная позиция. Отхождение ствола лёгочной артерии от левого желудочка. Отмечается митрально-легочное фиброзное продолжение.
Примечание: ЛЖ — левый желудочек, ЛА — лёгочная артерия.
Figure 4. Apical five-chamber view. Origin of the pulmonary artery trunk from the left ventricle. Mitral-pulmonary fibrous continuation is noted.
Note: LV — left ventricle, PA — pulmonary artery.
Заключение. ВПС: корригированная ТМС (L-транспозиция) (инверсия желудочков и дискордантная транспозиция Ао и ЛА). Умеренная недостаточность артериального (анатомически трикуспидального) клапана. Дилатация ЛП. Незначительная регургитация венозного (анатомически митрального) клапана. Косвенные признаки незначительного нарушения регионарной систолической функции ПЖ (артериального желудочка).
На основании результатов ЭхоКГ было принято решение о госпитализации в кардиологическое отделение для дообследования и лечения.
По данным холтеровского мониторирования ЭКГ (ХМЭКГ): правильный циркадный профиль ритма. Вариабельность ритма нормальная. В период бодрствования на фоне физической нагрузки зарегистрированы эпизоды синусовой тахикардии с максимальной ЧСС 150 ударов в минуту, сопровождающиеся депрессией сегмента ST в отведениях V5 и aVF на 0,5–1,3 мм. В период бодрствования зафиксированы 1 желудочковая и 8 наджелудочковых экстрасистол. Во время ночного сна выявлены короткие эпизоды преходящей АВ-блокады 1 степени. Всё время наблюдения регистрировались эпизоды выраженной синусовой аритмии.
Компьютерная томография органов грудной клетки. Транспозиция Ао (леворасположенная Ао). Венозный застой лёгких 1–2 степени.
Пациентке Э. была назначена симптоматическая терапия (торасемид, спироналоктон, метопролола сукцинат). На фоне проведенного лечения состояние больной улучшилось, в динамике одышка при физической нагрузке уменьшилась.
27.09.2019 г. пациентка Э. была выписана из стационара в удовлетворительном состоянии, даны рекомендации продолжить приём метопролола сукцината 50 мг утром под контролем АД и ЧСС, спироналоктона 25 мг утром и торасемида 5 мг утром под контролем АД, уровня калия и креатинина крови (контроль 1 раз в 3–6 месяцев) и диуреза. Кроме того, рекомендовано диспансерное наблюдение у кардиолога по месту жительства, проведение ХМЭКГ для исключения тяжёлой степени АВ-блокады и ЭхоКГ для мониторирования работы артериального ПЖ и степени недостаточности артериального (анатомически трикуспидального) клапана 1 раз в 12 месяцев.
Обсуждение
Пациентке Э., 1988 г. р., диагноз «ВПС: корригированная ТМС» впервые выставили в 31 год при проведении ЭхоКГ во время самообращения в стационар в связи с возникшей одышкой, продолжавшейся в течение двух месяцев. Возможно, отсутствие клинических проявлений и гемодинамических нарушений в течение длительного времени связано с тем, что у больной при наличии корригированной ТМС отсутствовали часто встречающиеся при этой патологии сопутствующие пороки: ДМПП, ДМЖП, ОАП, стеноз ЛА. На фоне имеющегося порока круги кровообращения физиологически функционировали верно. Жалобы, с которыми поступила пациентка, возможно, являются следствием постепенно развившейся недостаточности артериального (анатомически ТК) клапана, связанной с дисплазией ТК и функциональной неполноценностью морфологически ПЖ, не предназначенного для выполнения насосной функции и преодоления высокого сопротивления большого круга кровообращения. Недостаточность артериального клапана и регионарная систолическая дисфункция ПЖ, по-видимому, привели к застою в малом круге кровообращения, что и обусловило появление одышки.
В настоящее время пациентка Э. чувствует себя удовлетворительно, наблюдается у кардиолога по месту жительства. Больной ежегодно проводится трансторакальное ЭхоКГ обследование, по результатам которого отсутствует отрицательная динамика (степень недостаточности артериального клапана не увеличивается, глобальная сократимость ПЖ в норме), а также ХМЭКГ (АВ-блокады 2-й и 3-й степени не зарегистрированы). В течение всего периода наблюдения мониторируется уровень мозгового натрийуретического пептида, который сохраняется в переделах допустимых значений.
Прогноз пациентки относительно благоприятный. При развитии тяжёлой артериальной (трикуспидальной) недостаточности рекомендована хирургическая коррекция, при возникновении тяжёлой степени АВ-блокады — имплантация ЭКС.
Заключение
ТМС обычно проявляется с рождения в виде цианоза и одышки. Вариантом ТМС является редко встречающаяся корригированная транспозиция, которая часто сочетается с другими ВПС, требующими хирургической коррекции. Представленный клинический случай является крайне редким вариантом корригированной ТМС, проявившийся клинически только в зрелом возрасте. Основным методом диагностики ТМС является трансторакальная ЭхоКГ, верная интерпретация которого позволит поставить правильный диагноз.
Финансирование. Исследование не имело спонсорской поддержки.
Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов.
Список литературы
1. Армстронг У.Ф., Райан Т. Эхокардиография по Харви Фейгенбауму. М.: МЕДпресс-инфор; 2023.
2. Ассоциация сердечно-сосудистых хирургов России. Ассоциация детских кардиологов России. Российское кардиологическое общество. Транспозиция магистральных артерий. Клинические рекомендации. 2021.
3. Crainz F. The editions and translations of Dr. Matthew Baillie’s Morbid Anatomy. Med Hist. 1982;26(4):443-452. DOI: 10.1017/s0025727300041867
4. Банкл Г. Врожденные пороки сердца и крупных сосудов. М.: Книга по требованию; 2013.
5. Митина И.Н., Бондарев Ю.И. Неинвазивная ультразвуковая диагностика врожденных пороков сердца: Атлас. М.: Издательский дом Видар-М; 2004.
6. Шиллер Н.Б., Осипов М.А. Клиническая эхокардиография. Четвертое издание. М.: МЕДпресс-информ; 2023.
7. Lang RM, Badano LP, Mor-Avi V, Afilalo J, Armstrong A, Ernande L, et al. Recommendations for cardiac chamber quantification by echocardiography in adults: an update from the American Society of Echocardiography and the European Association of Cardiovascular Imaging. J Am Soc Echocardiogr. 2015;28(1):1-39.e14. DOI: 10.1016/j.echo.2014.10.003
8. Galderisi M, Cosyns B, Edvardsen T, Cardim N, Delgado V, Di Salvo G, et al. Standardization of adult transthoracic echocardiography reporting in agreement with recent chamber quantification, diastolic function, and heart valve disease recommendations: an expert consensus document of the European Association of Cardiovascular Imaging. Eur Heart J Cardiovasc Imaging. 2017;18(12):1301-1310. DOI: 10.1093/ehjci/jex244
Об авторах
С. Р. ГутоваРоссия
Саида Руслановна Гутова, к. м. н., доцент
кафедра факультетской терапии
Майкоп
В. В. Скибицкий
Россия
Виталий Викентьевич Скибицкий, д. м. н., профессор, заведующий кафедрой
кафедра госпитальной терапии
Краснодар
А. В. Фендрикова
Россия
Александра Вадимовна Фендрикова, к. м. н., доцент, доцент кафедры
кафедра госпитальной терапии
Краснодар
Дополнительные файлы
Рецензия
Для цитирования:
Гутова С.Р., Скибицкий В.В., Фендрикова А.В. Клинический случай установления диагноза корригированной транспозиции магистральных сосудов у пациентки в зрелом возрасте. Южно-Российский журнал терапевтической практики. 2025;6(1):81-87. https://doi.org/10.21886/2712-8156-2025-6-1-81-87
For citation:
Gutova S.R., Skibitsky V.V., Fendrikova A.V. A clinical case of diagnosis of the corrected transposition of the great arteries in an adult patient. South Russian Journal of Therapeutic Practice. 2025;6(1):81-87. (In Russ.) https://doi.org/10.21886/2712-8156-2025-6-1-81-87


























