Перейти к:
Влияние уровней гепарансульфата, VCAM-1 и ICAM-1 крови в совокупности с клиническими и морфологическими особенностями течения гломерулонефрита на вероятность достижения ремиссии
https://doi.org/10.21886/2712-8156-2021-2-3-86-93
Аннотация
Цель: анализ влияния молекул адгезии (ICAM-1, VCAM-1) и гепарансульфата крови в совокупности с клиникоморфологическими признаками на вероятность развития ремиссии при гломерулонефрите. Материал и методы: в исследование включено 80 больных гломерулонефритом в возрасте 35,7 ± 10,9 лет. Всем пациентам определяли сывороточные уровни ICAM-1, VCAM-1 и гепарансульфата методом количественного иммуноферментного анализа. Проводилась пункционная нефробиопсия с верификацией формы нефрита и определением признаков тубулоинтерстициального компонента (ТИК), тубулоинтерстициального воспаления (ТИВ), гломерулосклероза. Результаты: высокие значения гепарансульфата и мочевой кислоты в крови снижают вероятность достижения ремиссии при гломерулонефрите. Кроме того, высокие значения гепарансульфата в крови на фоне выраженного ТИК или ТИВ сопровождались снижением вероятности наступления ремиссии. Нарастание уровня ICAM-1 крови в совокупности с повышением возраста, уровня фибриногена в крови, а также нарастанием явлений ТИК, ТИВ и гломерулосклероза снижают вероятность достижения ремиссии при гломерулонефрите. Нарастание уровня VCAM-1 в крови на фоне повышения возраста пациента, гиперурикемии, нарастания явлений ТИВ, ТИК и гломерулосклероза также сопровождается снижением вероятности достижения ремиссии. Нами были составлены номограммы оценки прогноза развития ремиссии. Заключение: оценка уровней гепарансульфата, ICAM-1 и VCAM-1 в крови в совокупности с рядом клинико-морфологических признаков является важным инструментом прогнозирования эффективности терапии гломерулонефрита.
Ключевые слова
Для цитирования:
Батюшин М.М., Баяндурова К.М., Синельник Е.А. Влияние уровней гепарансульфата, VCAM-1 и ICAM-1 крови в совокупности с клиническими и морфологическими особенностями течения гломерулонефрита на вероятность достижения ремиссии. Южно-Российский журнал терапевтической практики. 2021;2(3):86-93. https://doi.org/10.21886/2712-8156-2021-2-3-86-93
For citation:
Batiushin M.M., Bayandurova K.M., Sinelnik E.A. The effect of blood levels of heparan sulfate, VCAM-1 and ICAM-1 in combination with clinical and morphological features of the course of glomerulonephritis on the probability of achieving remission. South Russian Journal of Therapeutic Practice. 2021;2(3):86-93. (In Russ.) https://doi.org/10.21886/2712-8156-2021-2-3-86-93
Вступление
При гломерулонефрите развитие эндотелиальной дисфункции является неотъемлемой частью патогенеза заболевания, а также определяет эффективность терапии и темпы прогрессирования нефрита. Оценка развития эндотелиальной дисфункции может включать в себя определение множества факторов. Особый интерес представляют молекулы сосудистой адгезии, такие как сосудистая молекула клеточной адгезии–1 (VCAM-1) и межклеточная молекула адгезии-1 (ICAM-1), поскольку они запускают процесс адгезии лейкоцитов и их миграцию в субэндотелиальное пространство, тем самым определяя роль эндотелиальной дисфункции в поддержании воспалительного процесса в почечной ткани при гломерулонефрите [1][2][3].
Гепарансульфат представляет собой белок, относящийся к группе протеогликанов, известный как профиброгенный фактор [4]. Он является важным структурным компонентом базальной мембраны и участвует в регуляции гломерулярной проницаемости. В последние годы появились исследования, демонстрирующие способность гепарансульфата повышать концентрацию лейкоцитов на эндотелии, ухудшая его функцию [5]. И молекулы адгезии, и гепарансульфат способны реализовать свой провоспалительный и эндотелиотоксичный потенциал на модели гломерулонефрита. Особый интерес представляет анализ их влияния на вероятность развития ремиссии при гломерулонефрите.
Цель исследования — анализ влияния молекул адгезии (ICAM-1, VCAM-1) и гепарансульфата крови в совокупности с клиникоморфологическими признаками на вероятность развития ремиссии при гломерулонефрите.
Материалы и методы
Протокол исследования был одобрен Локальным независимым этическим комитетом ФГБОУ ВО РостГМУ Минздрава России. Все больные подписали добровольное информированное согласие. Критериями включения были возраст больного от 18 до 80 лет, наличие нефротического или нефритического синдрома, первичного гломерулонефрита в стадии обострения до начала проведения иммуносупрессивной патогенетической терапии. Критериями невключения стали 5-я стадия ХБП с сопутствующими сахарным диабетом, ишемической болезнью сердца, хронической сердечной недостаточностью (ФК II-IV), обострением инфекции мочевых путей, наличием мочекаменной болезни, беременности, гепатита, психическими нарушениями, алкоголизмом.
Исследование включало два этапа. Первый этап — одномоментное когортное исследование, во время которого осуществлялись сбор данных анамнеза заболевания, физическое и лабораторное обследование, изучение медицинской документации, стационарное лечение в соответствии с клиническими рекомендациями Ассоциации нефрологов. Второй этап заключался в когортном проспективном 12-месячном наблюдении за больными с повторным физическим и лабораторным обследованием, оценкой развития ремиссии заболевания по критериям, изложенным в клинических рекомендациях ассоциации нефрологов.
Было включено 80 больных в возрасте 35,7 ± 10,9 лет. Скорость клубочковой фильтрации (СКФ) рассчитывали по формуле CKD-EPI (Chronic Kidney Desease Epidemiology Collaboration). В 80% случаев встречались пациенты с нормальной фильтрационной функцией почек, тогда как у 20% она была снижена. Всем больным была выполнена чрескожная нефробиопсия с целью верификации морфологического варианта гломерулонефрита. Распределение больных по морфологическому варианту было следующим: IgА-нефропатия — 44 пациента, фокальносегментарный гломерулосклероз — 16 пациентов, мембранозная нефропатия и болезнь минимальных изменений — по 10 пациентов, IgМ-нефропатия и мембранопролиферативный глосмерулонефрит — по 2 пациента. Нефритический синдром встречался у 62,5% больных, нефротический — у 37,5%. Также оценивали признаки тубулоинтерстициального компонента (ТИК) и тубулоинтерстициального воспаления (ТИВ) и их выраженность в рангах.
Всем пациентам определяли сывороточные уровни ICAM-1 (intercellular adhesion molecule 1), VCAM-1 (vascular cell adhesion molecule 1) и гепарансульфат методом количественного иммуноферментного анализа (ИФА) (Luminex MAGPIX, США). В утренние часы натощак производился забор венозной крови в вакутайнеры, далее полученные биообразцы охлаждались при температуре –20°С и центрифугировались со скоростью 1000 об/мин перед выполнением анализа.
Статистический анализ проводился с помощью программ Microsoft Office Excel 2010 (Microsoft Corp., США) и «STATISTICA 10.0» (StatSoft Inc., США). В данной части исследования применялся логист-регрессионный анализ с расчетом относительных рисков (OR) и определением χ2, при значении р <0,05 связь считалась статистически значимой.
ROC-анализ (Receiver Operating Characteristic curve) с конструированием операционных характеристических кривых и определением коэффициента площади кривой (AUC) применялся для оценки диагностической (прогностической) информативности используемых методов. Информативность считалась отличной при значении AUC 0,9 – 1,0, очень хорошей — при 0,8 – 0,9, хорошей — при 0,7 – 0,8, средней — при 0,6 – 0,7, неудовлетворительной — при 0,5 – 0,6.
Результаты
Данная статья является фрагментом научного исследования, в рамках которого изучалось именно комбинированное влияние уровней гепарансульфата, ICAM-1 и VCAM-1 крови в совокупности с рядом клинических и морфологических признаков на вероятность развития полной или частичной ремиссии (ПР, ЧР) или отсутствия ремиссии (ОР). С этой целью был применён логит-регрессионный анализ. В ходе исследования были получены данные о влиянии исходного уровня гепарансульфата и ряда клинико-морфологических признаков на достижение ремиссии заболевания в течение 12 месяцев наблюдения (табл. 1).
Таблица 1
Результаты логит-регрессионного анализа влияния гепарансульфата в совокупности с клинико-морфологическими показателями на вероятность достижения ремиссии гломерулонефрита (ПР+ЧР против ОР) (только статистически значимые результаты)
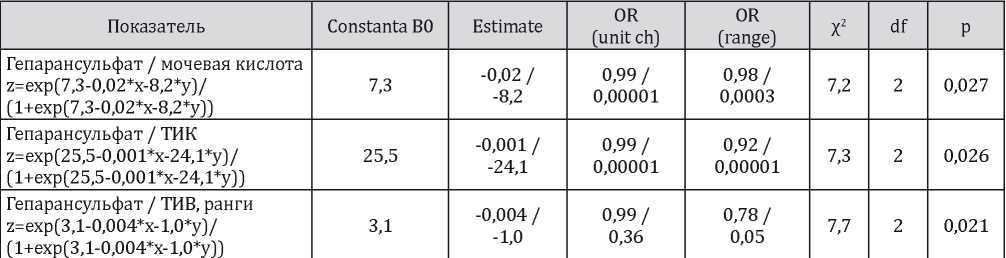
Примечание: ТИК — тубулоинтерстициальный компонент, ТИВ — тубулоинтерстициальное воспаление
Показано, что высокие значения гепарансульфата и мочевой кислоты в крови снижают вероятность достижения ремиссии при гломерулонефрите. Также высокие значения гепарансульфата в крови на фоне выраженного ТИК или ТИВ сопровождались снижением вероятности наступления ремиссии.
В качестве примера на рис. 1 представлен график зависимости ремиссии от исходных уровней мочевой кислоты и гепарансульфата.
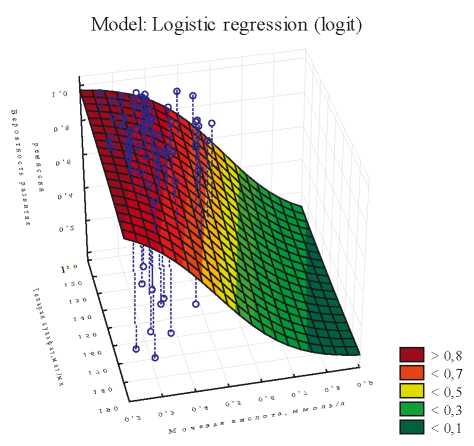
Рисунок 1. График логист-регрессии вероятности развития ремиссии в зависимости от уровня гепарансульфата и мочевой кислоты крови.

Рисунок 2. График вероятности развития ремиссии гломерулонефрита в зависимости от уровня ICAM-1 и выраженности ТИВ.
На основании полученных уравнений логистрегрессии была составлена номограмма оценки прогноза развития ремиссии гломерулонефрита (табл. 2).
Таблица 2
Номограмма оценки развития ремиссии в течение 12 месяцев в зависимости от исходного уровня гепарансульфата крови и других признаков
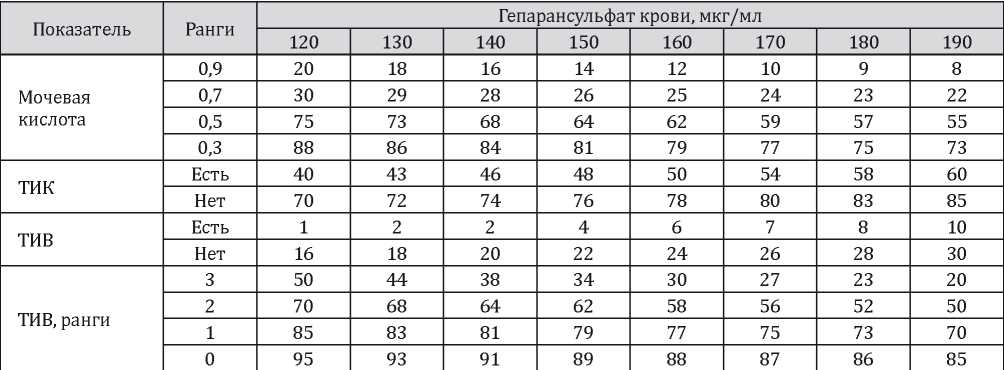
Проведенный логист-регрессионный анализ позволил также продемонстрировать роль ICAM-1 крови в совокупности с другими клинико-морфологическими признаками в развитии ремиссии гломерулонефрита (табл. 3).
Таблица 3
Результаты логист-регрессионного анализа влияния ICAM-1 крови и клиниколабораторных признаков на вероятность достижения ремиссии (ПР+ЧР против ОР) (только статистически значимые результаты)
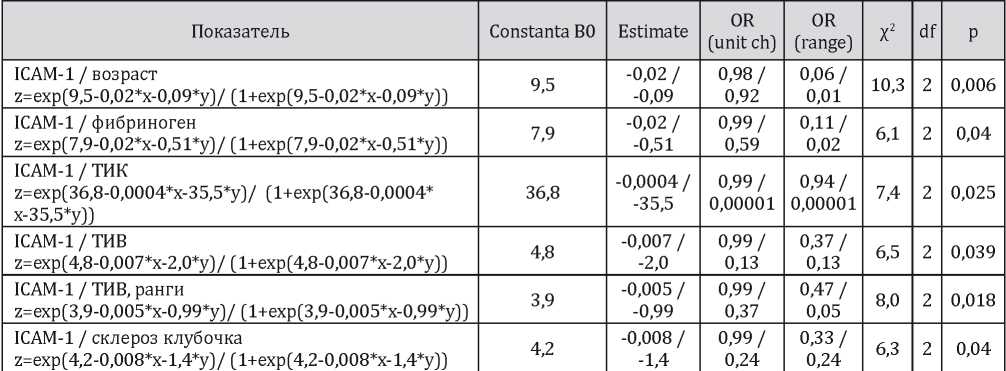
Было показано, что нарастание уровня ICAM-1 крови в совокупности с повышением возраста, уровня фибриногена в крови, а также нарастанием явлений ТИК, ТИВ и гломерулосклероза снижают вероятность достижения ремиссии при гломерулонефрите.
В качестве примеров на рис. 2 и 3 представлены графики зависимости наступления ремиссии от исходного уровня ICAM-1 в сочетании с выраженностью ТИВ или уровней фибриногена крови.
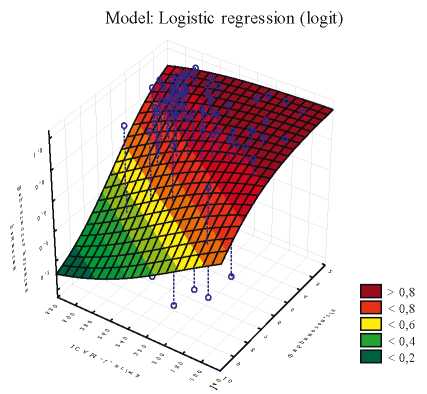
Рисунок 3. График вероятности развития ремиссии гломерулонефрита в зависимости от уровня ICAM-1 и фибриногена.
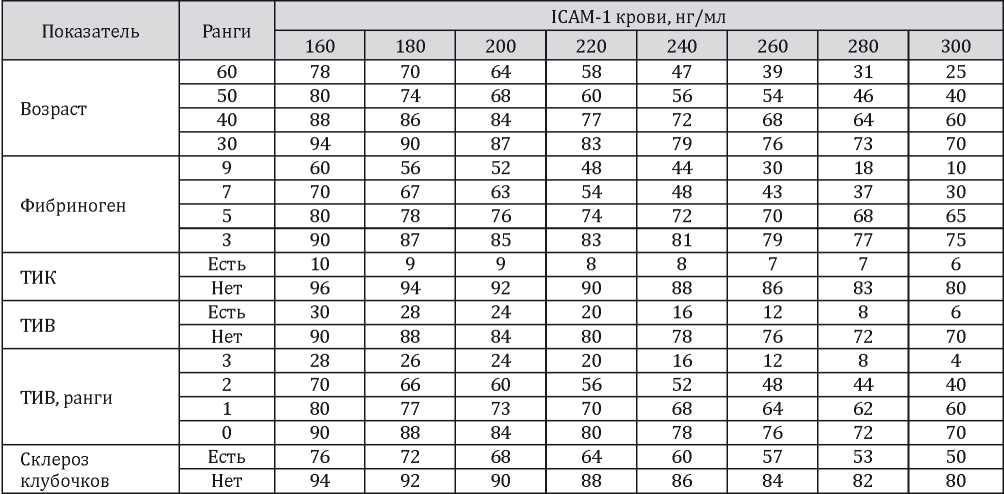
По результатам логист-регрессионного анализа была составлена номограмма оценки риска развития ремиссии на основании исходных данных с включением в их число уровней ICAM-1 (табл. 4).
Таблица 4
Номограмма оценки вероятности развития ремиссии в течение 12 месяцев в зависимости от исходного уровня ICAM-1 и других признаков
При дальнейшем проведении логистрегрессионного анализа оценивалось влияние VCAM-1 в крови в совокупности с клиникоморфологическими признаками на вероятность достижения ремиссии (табл. 5).
Таблица 5
Результаты логист-регрессионного анализа влияния клинико-лабораторных показателей на вероятность достижения ремиссии (ПР+ЧР против ОР) (только статистически значимые результаты)
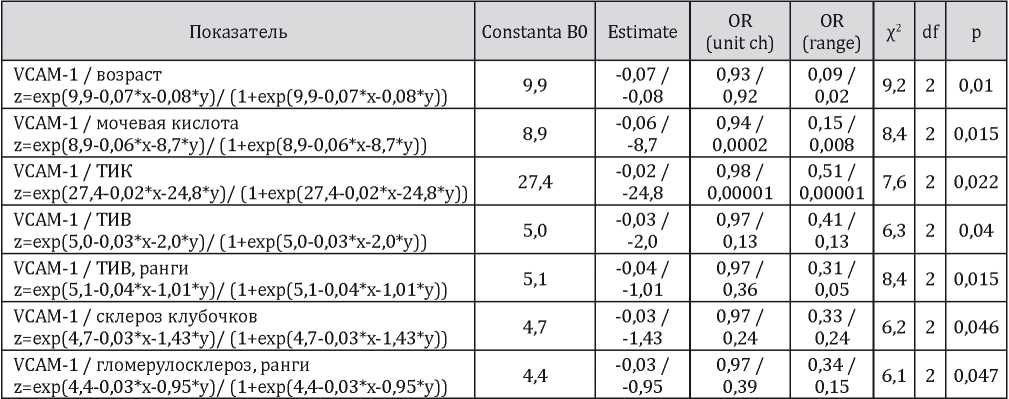
В исследовании показано, что нарастание уровня VCAM-1 в крови на фоне повышения возраста пациента, гиперурикемии, нарастания явлений ТИВ, ТИК и гломерулосклероза сопровождается снижением вероятности достижения ремиссии. В качестве примера такого влияния на рис. 4 представлен график зависимости развития ремиссии от исходных уровней VCAM-1 и мочевой кислоты крови.

Рисунок 4. График вероятности развития ремиссии в зависимости от уровня VCAM-1 и мочевой кислоты крови.
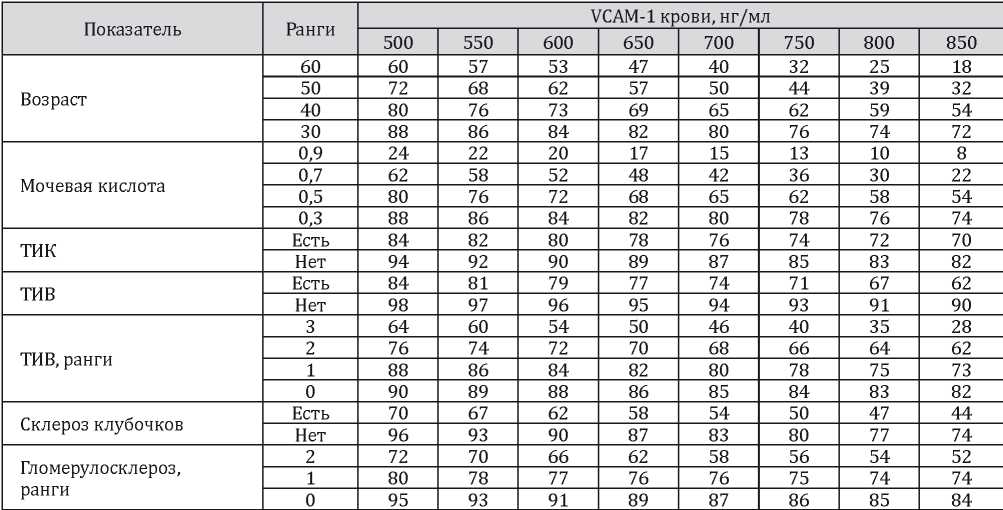
Полученные уравнения регрессии легли в основу номограммы оценки развития вероятности ремиссии гломерулонефрита у обследуемых больных. (табл. 6).
Таблица 6
Номограмма оценки развития ремиссии в течение 12 месяцев в зависимости от исходного уровня VCAM-1 и других признаков
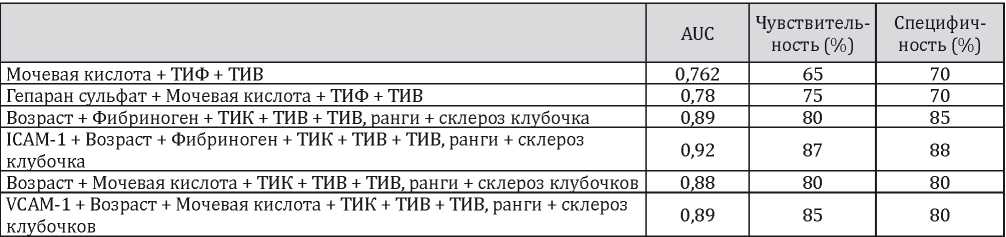
Полученные уравнения регрессии и номограммы приобрели большую информативность в силу включения гепарансульфата, ICAM-1 и VCAM-1 в сравнении с традиционными инструментами прогнозирования, тем самым повышая персонифицированность прогноза. Это видно из проведенного ROC-анализа (табл. 7). В частности, введение в модель прогнозирования гепарансульфата повышало информативность прогноза на 10% за счёт роста чувствительности, а включение ICAM-1 в модель прогнозирования повышало информативность прогноза за счет специфичности на 3% и чувствительности на 7%. Включение в модель прогнозирования VCAM-1 повышало информативность за счёт чувствительности на 5%.
Таблица 7
Результаты ROC-анализа оценки информативности методов прогнозирования ремиссии хронического гломерулонефрита
Обсуждение
В результате проведённого исследования были получены номограммы на основе уравнений логит-регрессии. Оценка данных факторов в совокупности поможет определить риск развития ремиссии у больных с гломерулонефритом (рис. 5).
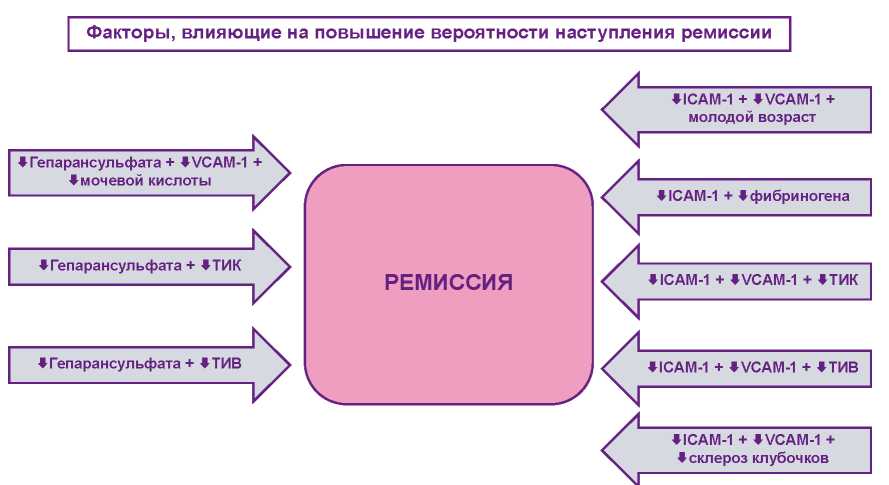
Рисунок 5. Влияние уровней ICAM-1, VCAM-1 и гепарансульфата крови в совокупности с другими факторами на развитие ремиссии гломерулонефрита.
Нами обнаружены единичные исследования, демонстрирующие влияние гепарансульфата, ICAM-1 и VCAM-1 на вероятность развития ремиссии [6][7][8]. Однако работ, посвящённых воздействию этих факторов на развитие воспалительного процесса в почках, альбуминурии, довольно много [9][10]. Очевидно, что влияние молекул адгезии и гепарансульфата на развитие эндотелиальной дисфункции и реализацию её провоспалительного потенциала при гломерулонефрите гипотетически должно оказывать воздействие не только на тяжесть течения нефрита, но и на прогноз развития ремиссии. В нашем исследовании помимо молекул адгезии и гепарансульфата в анализ включались и те факторы, наличие и выраженность которых очевидно представляет угрозу формирования ремиссии. Комплексная оценка вероятности достижения ремиссии определяет вектор персонифицированного подхода к ведению больного с гломерулонефритом, а оценка плазменных факторов позволяет предложить в перспективе альтернативу пункционной нефробиопсии в качестве основного метода не только классификации гломерулонефрита, но и определение прогноза его течения [11].
Заключение
В нашем исследовании было показано, что повышение уровней гепарансульфата в крови в совокупности с гиперурикемией, ТИВ и ТИК сопровождается снижением вероятности достижения ремиссии при гломерулонефрите. Повышение уровней ICAM-1 вместе с гиперфибриногенемией, выраженными ТИК, ТВ и гломерулосклерозом также сопровождается снижением вероятности достижения ремиссии. Повышение уровня VCAM-1 в крови в совокупности с гиперурикемией, выраженным ТИК, ТИВ и гломерулосклерозом приводит с снижению вероятности достижения ремиссии при гломерулонефрите.
Список литературы
1. Bui T.M., Wiesolek H.L., Sumagin R. ICAM-1: A master regulator of cellular responses in inflammation, injury resolution, and tumorigenesis. J Leukoc Biol. 2020;108(3):787-799. DOI: 10.1002/JLB.2MR0220-549R.
2. Regal-McDonald K., Somarathna M., Lee T., Litovsky S.H., Barnes J., Peretik J.M., et al. Assessment of ICAM-1 N-glycoforms in mouse and human models of endothelial dysfunction. PLoS One. 2020;15(3):e0230358. DOI: 10.1371/journal.pone.0230358.
3. van Wetering S., van den Berk N., van Buul J.D., Mul F.P., Lommerse I., Mous R., et al. VCAM-1-mediated Rac signaling controls endothelial cell-cell contacts and leukocyte transmigration. Am J Physiol Cell Physiol. 2003;285(2):C343-52. DOI: 10.1152/ajpcell.00048.2003.
4. Borza D.B. Glomerular basement membrane heparan sulfate in health and disease: A regulator of local complement activation. Matrix Biol. 2017;57-58:299-310. DOI: 10.1016/j.matbio.2016.09.002.
5. Xu D., Fuster M.M., Lawrence R., Esko J.D. Heparan sulfate regulates VEGF165- and VEGF121-mediated vascular hyperpermeability. J Biol Chem. 2011;286(1):737-45. DOI: 10.1074/jbc.M110.177006.
6. Burhan I., Furini G., Lortat-Jacob H., Atobatele A.G., Scarpellini A., Schroeder N., et al. Interplay between transglutaminases and heparan sulphate in progressive renal scarring. Sci Rep. 2016;6:31343. DOI: 10.1038/srep31343.
7. Moon K.C., Park S.Y., Kim H.W., Hong H.K., Lee H.S. Expression of intercellular adhesion molecule-1 and vascular cell adhesion molecule-1 in human crescentic glomerulonephritis. Histopathology. 2002;41(2):158-65. DOI: 10.1046/j.1365-2559.2002.01446.x.
8. Arrizabalaga P., Solé M., Abellana R., de las Cuevas X., Soler J., Pascual J.,et al. Tubular and interstitial expression of ICAM-1 as a marker of renal injury in IgA nephropathy. Am J Nephrol. 2003;23(3):121-8. DOI: 10.1159/000068920.
9. Rops A.L., van der Vlag J., Lensen J.F., Wijnhoven T.J., van den Heuvel L.P., van Kuppevelt T.H., et al. Heparan sulfate proteoglycans in glomerular inflammation. Kidney Int. 2004;65(3):768-85. DOI: 10.1111/j.1523-1755.2004.00451.x.
10. Raats C.J., Van Den Born J., Berden J.H. Glomerular heparan sulfate alterations: mechanisms and relevance for proteinuria. Kidney Int. 2000;57(2):385-400. DOI: 10.1046/j.1523-1755.2000.00858.x.
11. Lees G.E., Cianciolo R.E., Clubb F.J. Jr. Renal biopsy and pathologic evaluation of glomerular disease. Top Companion Anim Med. 2011;26(3):143-53. DOI: 10.1053/j.tcam.2011.04.006.
Об авторах
М. М. БатюшинРоссия
Батюшин Михаил Михайлович, проф., д.м.н., профессор кафедры внутренних болезней №2
Ростов-на-Дону
К. М. Баяндурова
Россия
Баяндурова Карина Михайловна, к.м.н., врач-нефролог урологического центра
Ростов-на-Дону
Е. А. Синельник
Россия
Синельник Елена Александровна, к.м.н., доцент кафедры патологической анатомии
Ростов-на-Дону
Дополнительные файлы
Рецензия
Для цитирования:
Батюшин М.М., Баяндурова К.М., Синельник Е.А. Влияние уровней гепарансульфата, VCAM-1 и ICAM-1 крови в совокупности с клиническими и морфологическими особенностями течения гломерулонефрита на вероятность достижения ремиссии. Южно-Российский журнал терапевтической практики. 2021;2(3):86-93. https://doi.org/10.21886/2712-8156-2021-2-3-86-93
For citation:
Batiushin M.M., Bayandurova K.M., Sinelnik E.A. The effect of blood levels of heparan sulfate, VCAM-1 and ICAM-1 in combination with clinical and morphological features of the course of glomerulonephritis on the probability of achieving remission. South Russian Journal of Therapeutic Practice. 2021;2(3):86-93. (In Russ.) https://doi.org/10.21886/2712-8156-2021-2-3-86-93


























