Перейти к:
Ошибки диагностики и сложности ведения пациентов с алкогольным поражением сердца
https://doi.org/10.21886/2712-8156-2022-3-2-100-106
Аннотация
Освещены трудности диагностики и ведения пациентов с алкоголь-индуцированным поражениям сердца, особенности клиники алкогольной кардиомиопатии. Избыточное и длительное потребление алкоголя увеличивает риск развития острой и хронической сердечной недостаточности, нарушений ритма сердца и утяжеляет уже имеющиеся сердечно-сосудистые заболевания. При этом из-за недостаточной оценки происхождения кардиальных проявлений (пациенты нередко скрывают или преуменьшают факт злоупотребления алкоголем) больные не всегда получают специфическое лечение. Ведение таких пациентов представляет значительные трудности, учитывая в том числе поражение желудочно-кишечного тракта, центральной и периферической нервной системы, оно должно осуществляться совместно с врачами других специальностей.
Ключевые слова
Для цитирования:
Тарловская Е.И., Соловьёва Е.В., Попова Н.А., Власова Т.В., Горбунова М.Л., Идабаева Н.В., Почукалина Ю.А. Ошибки диагностики и сложности ведения пациентов с алкогольным поражением сердца. Южно-Российский журнал терапевтической практики. 2022;3(2):100-106. https://doi.org/10.21886/2712-8156-2022-3-2-100-106
For citation:
Tarlovskaya E.I., Solovyova E.V., Popova N.A., Vlasova T.V., Gorbunova M.L., Idabaeva N.V., Pochukalina Yu.A. A clinical case of arrhythmogenic right ventricular dysplasia (ADP). South Russian Journal of Therapeutic Practice. 2022;3(2):100-106. (In Russ.) https://doi.org/10.21886/2712-8156-2022-3-2-100-106
В России, согласно данным ВОЗ, злоупотребляет алкоголем около 5% населения в возрасте старше 18 лет, что составляет порядка 7,5 млн человек. Несмотря на определенную положительную тенденцию, сформировавшуюся за последние 3–5 лет в отношении алкоголизации населения, данная проблема всё ещё стоит достаточно остро. При этом в России чаще употребляют крепкие спиртные напитки (39%), тогда как в других европейских странах предпочтение отдается пиву и вину. Следует также отметить высокий уровень потребления алкоголя среди женщин в России по сравнению с европейскими странами [1][2].
Этанол и его активный метаболит ацетальдегид оказывают системное токсическое действие на организм. Сердечно-сосудистая система после печени и желудочно-кишечного тракта является второй наиболее пострадавшей системой от токсичности этанола.
При высокой дозе (более 60 г/сут. для мужчин и 40 г/сут. для женщин) и хроническом потреблении (обычно более 10 лет) возможно развитие алкогольной болезни сердца — группы заболеваний сердца, общим для которых является избирательное повреждение миокарда продуктами метаболизма этанола [3].
Последствиями влияния хронического злоупотребления алкоголем на сердечно-сосудистую систему могут быть дисфункция желудочков и предсердий, аритмии, алкогольная кардиомиопатия, в том числе с проявлениями сердечной недостаточности (СН), артериальная гипертензия (АГ), коронарный и периферический атеросклероз, повышенный риск всех форм инсульта [4].
Основными механизмами кардиопатогенного действия являются влияние на энергоснабжение клетки, прямое токсическое действие этанола и ацетальдегида, нарушение связи между сокращением и возбуждением, повреждение свободными радикалами, нарушение липидного обмена, дисбаланс катехоламинов и ионов. Эти механизмы приводят к развитию СН, которая характеризуется нарушением структуры сократительного аппарата кардиомиоцитов и их функциональной асимметрией. Длительное употребление алкоголя в больших количествах вызывает неблагоприятные гистологические, клеточные и структурные изменения в миокарде. В патогенезе алкогольной кардиомиопатии (АКМП) могут играть роль иммунологические нарушения и воспаление [5].
При длительном (более 20 лет высокого потребления этанола) при кумулятивных пожизненных дозах, превышающих 20 кг этанола/кг массы тела, что эквивалентно 180 напиткам в месяц, механизмы восстановления сердца ограничены. Развивается диффузный некроз миоцитов, которые замещаются интерстициальным фиброзом и компенсаторной гипертрофией оставшихся миоцитов [3].
Всё это в итоге приводит к дилатации полости левого желудочка (ЛЖ) сердца, снижению его сократительной способности с последующим развитием СН. В развитии АКМП, кроме непосредственного токсического действия этанола и его метаболитов на миокард, значительную роль играют нейроэндокринные нарушения, другие проявления алкогольной болезни (в том числе цирроз печени), генетическая предрасположенность сопутствующие электролитные нарушения (магний, фосфор, калий).
Прекращение потребления алкоголя может улучшить прогноз пациентов. У субъектов, которые продолжают пить в умеренных или высоких дозах (более 60 г этанола в день у мужчин, что эквивалентно четырём стандартным напиткам, и 40 г этанола в день у женщин, что эквивалентно 2,5 стандартным напиткам) развиваются прогрессирующие функциональные и структурные нарушения сердца с повторяющимися эпизодами сердечной недостаточности или рефрактерной застойной недостаточностью, аритмиями, которые обычно и являются причиной летального исхода [3][6].
Нарушения сердечного ритма типичны для пациентов, злоупотребляющих алкоголем, они могут быть одним из проявлений АКМП, усугубляя проявления СН и ухудшая её прогноз. Потенциальные проаритмические эффекты высоких концентраций этанола зависят, в том числе от ранее существовавших структурных и электрофизиологических нарушений (фиброз, дилатация, метаболический ацидоз). Взаимосвязь между хроническим употреблением алкоголя и аритмиями — это сложные взаимодействия между дозой, характером употребления алкоголя, возрастом и полом.[4]
Причинами аритмий являются следующие:
- повышенный выброс норадреналина и его непрерывная циркуляция, вегетативный дисбаланс, снижение вариабельности сердечного ритма, уменьшение чувствительности барорецепторов;
- электролитные нарушения;
- миокардиосклероз с развитием субстрата для аритмий по механизму re-entry;
- электрофизиологические изменения в клетках предсердий и желудочков: замедление внутрипредсердной проводимости, укорочение рефрактерного периода, отрицательное инотропное действие из-за ингибирования Са-каналов.
Электролитные нарушения часто встречаются у хронических алкоголиков как при острой алкогольной интоксикации, так и при алкогольной абстиненции и могут быть обусловлены прямым воздействием алкоголя или же быть вторичными по отношению к алкогольным заболеваниям, поражающим другие органы.
Гипокалиемия и гипомагнезиемия возникают вследствие недоедания, нарушенного всасывания, потерь через желудочно-кишечный тракт (рвота, диарея, алкогольный кетоацидоз) или с мочой, вторичного гиперальдостеронизма (при циррозе печени).
К алкоголь-индуцированным аритмиям относятся синусовая тахикардия (ассоциирована с острым приемом алкоголя, встречается у 25,9% пациентов вследствие вегетативного дисбаланса), фибрилляция и трепетания предсердий (ФП и ТП), парокизмальная предсердная и атрио-вентрикулярная тахикардия, частая суправентрикулярная и желудочковая экстрасистолия, пароксизмальная желудочковая тахикардия, внезапная смерть при постоянном употреблении алкоголя в большом количестве. Дефицит Mg сопряжен с удлинением интервала Q-T, желудочковыми нарушениями ритма, в том числе с torsades de pointes [7]. Сердечные аритмии могут возникнуть в период абстиненции из-за увеличения симпатической активности сердца и уменьшения вариабельности сердечного ритма.
ФП нередко провоцируется приёмом алкоголя, в том числе первый её пароксизм — «синдром праздничного сердца». Число желудочковых сокращений при ФП/ТП может иметь высокую частоту (180/мин. и выше) вследствие короткого рефрактерного периода правого предсердия. Воздержание от употребления алкоголя значительно снижает частоту эпизодов ФП [4].
У лиц, злоупотребляющих алкоголем (21–35 доз/нед.), по сравнению с умеренным его потреблением (2–6 доз/нед.) повышен риск желудочковой тахикардии и внезапной сердечной смерти, в том числе из-за возможного удлинения интервала QT [8].
Желудочковые нарушения ритма возрастают и в период абстиненции. Психоактивные препараты, которые принимают пациенты с алкогольной зависимостью, также могут удлинять интервал QT (трициклические антидепрессанты, селективные ингибиторы обратного захвата серотонина, препараты лития – «коктейль de la mort!») [8].
К сожалению, на сегодняшний день факт злоупотребления алкоголем как причина поражения сердечно-сосудистой системы выявляется достаточно поздно, что приводит к неадекватному ведению пациентов и ухудшению прогноза. Приводим собственное наблюдение.
Пациентка В., 57 лет, руководитель подразделения крупного банка, поступила в кардиологическое отделение с жалобами на одышку при незначительной физической нагрузке, усиливающуюся в положении лежа, отёки нижних конечностей, ощущение сердцебиения, «перебоев» в работе сердца, сжимающие боли за грудиной без иррадиации продолжительностью до 30 мин., возникающие как при нагрузке, так и в покое, проходящие самостоятельно, слабость, отсутствие аппетита. Вышеописанные симптомы появились впервые в последние 2 недели с быстрым прогрессированием. К врачу не обращалась. Со слов пациентки, подобное состояние — впервые.
В анамнезе гипертоническая болезнь (ГБ) в течение 7 лет с повышением АД до 170/100 мм рт. ст., регулярно не лечится, иногда принимает капотен. Замужем, 1 роды, менопауза с 53 лет. Последние 3 года получает менопаузальную гормональную терапию по рекомендации гинеколога из-за выраженных приливов. Наследственность не отягощена. Вредные привычки отрицает.
Объективно. Состояние средней степени тяжести, достаточного питания, ИМТ 26г/м2. Кожные покровы чистые, бледноваты, цианоз губ. В лёгких в нижне-задних отделах с обеих сторон умеренное количество влажных хрипов, частота дыхания — 26 в мин. Границы сердца не расширены. Тоны сердца значительно приглушены, систолический шум на верхушке, фибрилляция предсердий со средним числом сердечных сокращений (ЧСС) — 164 в мин., частые экстрасистолы. АД d=s 100/60 мм рт. ст.
Язык обложен белым налётом. Живот несколько вздут, мягкий, чувствительный в правом подреберье, печень +3 см из-подреберья, край её плотноват. Селезёнка не увеличена. Пастозность нижних конечностей.
Результаты лабораторных исследований: общеклинический анализ крови, коагулограмма и общий анализ мочи (уд. вес 1015–1018) — без особенностей.
Биохимический анализ крови: тропонин I — 0,40 нг/мл (< 0,5; здесь и далее в скобках указаны референсные интервалы); калий — 3,5 ммоль/л (3,5–5,2); натрий — 143,5 ммоль/л (136–145); общ. белок — 55,0 г/л (55,0–75,0); альбумин — 23 г/л (25,0–39,0); креатинин — 74,0 мкмоль/л (50–98); мочевина — 6,5 ммоль/л (2,5–6,7); скорость клубочковой фильтрации (формула CKD EPI) — 78 мл/мин.; билирубин общ. — 26,0 мкмоль/л (1,7–21,0); билирубин прямой — 5,0 мкмоль\л (0,0–5,50); АлАТ — 68 мкмоль/л (7–41); ; АсАТ — 48 мкмоль/л (10–38 ); КФК — 130 МЕ (< 130); глюкоза — 4,73 ммоль/л (3,9–6,1). Т4, ТТГ — N; ХС общ. — 5,8 ммоль/л; ХС ЛПНП — 2,4 ммоль/л; ТГ — 2,5 ммоль/л.
Острофазовые реакции отрицательные (исключался миокардит).
Рентгенография органов грудной клетки: воспалительных и очаговых изменений не выявлено. Плевральные синусы свободны. Лёгочный рисунок усилен, преимущественно в базальных отделах. Корни лёгких несколько расширены. Сердце расположено нормально, размеры не увеличены. Сосудистый пучок не изменен. Аорта без особенностей. Верхняя полая вена не расширена. Диафрагма без особенностей.
На ЭКГ при поступлении: тахисистолическая форма фибрилляции предсердий с (ЧСС) 124–180 уд./мин., частая политопная желудочковая экстрасистолия. Гипертрофия левых отделов сердца, выраженные диффузные изменения процессов реполяризации желудочков. ЭКГ с прикроватного монитора представлено на рис. 1.
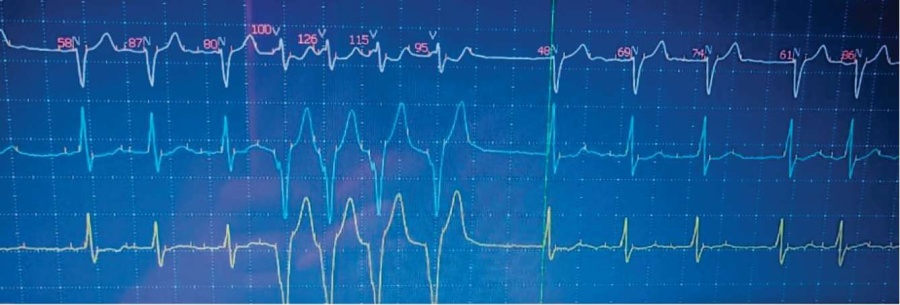
Рисунок 1. ЭКГ мониторирование больной В. в первые сутки (до восстановления синусового ритма): «пробежка» желудочковой тахикардии с частотой 212 уд./мин.
По данным трансторакальной эхокардиографии (выполнено после восстановления синусового ритма, ЧСС — 82 уд./мин.), выявлено увеличение левого предсердия (ЛП) — 4,20 см, индекса конечно-систолического объёма ЛП (ИКСО) — 34 мл/м2; умеренная гипертрофия левого желудочка (ЛЖ), задняя стенка ЛЖ (ЗСЛЖ) — 1,2 см; межжелудочковая пергородка (МЖП) — 1,2 см; увеличение индекса массы миокарда ЛЖ- ИММЛЖ — 122 г/м2 (N для женщин — до 95г/м2). Полости ЛЖ и правого желудочка (ПЖ) не расширены. Конечно-систолический размер (КСР) ЛЖ — 3,2 см; конечно-диастолический размер (КДР) ЛЖ — 5,2 см; КСО-конечно-систолический объем (КСО) ЛЖ — 40 мл; КДО-конечно-диастолический объем (КДО) ЛЖ — 122 мл; передне-задний размер ПЖ — 2,6/3,2 см (N из парастернальной позиции — до 3,0 см, из четырёхкамерной позиции N — до 3,8 см). Систолическая функция ЛЖ — на нижней границе N-ФВ, фракция выброса ЛЖ — 52% (по Simpson). Систолическая функция ПЖ — на нижней границе N (TAPSE 16 мм (N — более 16 мм), скорость S волны тканевого допплера — 11 см/с (N — более 10 см/с). Зоны гипо- и акинезии (дискинезии) не выявлены. Регургитация на митральном клапане 1 ст., клапан не изменен. Фиброз аорты. Признаки лёгочной гипертензии (систолическое давление в легочной артерии (СДЛА)) — 34 мм рт. ст. (недостаточность трикуспидального клапана 1–2 ст., максимальный градиент трикуспидальной регургитации — 19 мм рт. ст., нижняя полая вена не расширена, на вдохе спадение менее 20%). Диастолическая дисфункция левого желудочка по типу замедления релаксации (Е/А — 0,70, DT — 250 мс, E/E’ — 12, скорость латерального Е’ — 9,5 см/с).
Диагностическая коронарография: данных о гемодинамически значимых стенозах коронарных артерий не получено.
В 1-е сутки госпитализации синусовый ритм восстановился после введения амиодарона, препаратов калия, но сохранялась синусовая тахикардия с ЧСС 96 уд./мин. с частыми политопными экстрасистолами. На фоне терапии лечение сердечной недостаточности: иАПФ, бета-блокаторы, антагонисты альдостерона, мочегонные; состояние пациентки значительно улучшилось: исчезли одышка и периферические отеки, в лёгких дыхание везикулярное, дых. 16 в 1 мин., тоны сердца ритмичные, ЧСС 68 уд./мин., печень + 1 см из подреберья, появился аппетит.
Холтеровское ЭКГ мониторирование: исследование проводилось в течение 22 часов. За сутки зафиксирован синусовый ритм. Средняя ЧСС — 88 уд./мин., ЧСС минимальная — 56 уд/./мин., во время сна, ЧСС максимальная 126 — уд./мин. Желудочковая эктопическая активность представлена 3412 полиморфной желудочковой экстрасистолией (ЖЭС), преимущественно в дневное время. Одиночных — 3308, по типу бигеминии — 51, парных — 36. Пауз не выявлено. Выявлено 3 безболевых эпизода горизонтальной депрессии сегмента ST глубиной до 2 мм, max продолжительность — 7 мин., возникающих как в покое, так и во время ходьбы.
УЗИ органов брюшной полости: признаки жирового гепатоза.
Диагноз: ИБС: микроциркуляторная стенокардия. Пароксизмальная фибрилляция предсердий. Политопная желудочковая экстрасистолия. СНсФВ IIIФК (ХСН IIБ). Гипертоническая болезнь, корригированная. Риск IV.
Вместе с тем, причина СН оставалась неясной: наличие нестойкой артериальной гипертензии, отсутствие гемодинамически значимых стенозов коронарных артерий по данным коронароангиографии, исключение иной патологии сердца не могли объяснить её тяжесть при поступлении. Больная была выписана в удовлетворительном состоянии, ФК ХСН II с рекомендациями постоянного приема иАПФ, бета-блокаторов, антагонистов альдостерона, статинов. В дальнейшем чувствовала себя хорошо, вела активный образ жизни, много путешествовала, в том числе в жаркое время года. Лекарственные препараты не принимала, приступов аритмии не отмечала. Через 1 год вновь была госпитализирована в экстренном порядке в связи с декомпенсацией сердечной недостаточности. Кроме прежних жалоб (одышка в покое, сердцебиение, отёки ног, ощущение жжения за грудиной) отмечает выраженное «жжение» и похолодание в области стоп, ощущение «ватных ног», «онемения пальцев», «ползания мурашек», судороги икроножных мышц, неустойчивость при ходьбе, резкое ухудшение памяти, похудание на 7 кг за 0,5 года. При осмотре, по сравнению с предыдущей госпитализацией, обращало внимание резкое снижение мышечной массы верхних и нижних конечностей, выраженный акроцианоз, субиктеричность склер и кожных покровов, значительное увеличение печени +5 см из подреберья, край её плотноват. Вновь зарегистрирован пароксизм фибрилляции предсердий с высокой частотой ЧСС — до 180 уд./мин. (купирована в 1-е сутки амиодароном), АД 120/80 мм рт.ст. На 2-й день госпитализации развился гипертонический криз с повышением АД до 240/110 мм рт.ст. с выраженными вегетативными проявлениями: тахикардия до 160 уд./мин., дрожь во всём теле, возбуждение, покраснение лица.
На ЭКГ после восстановления ритма диффузные изменения в виде сглаженных и слабо-отрицательных зубцов T.
По данным трансторакальной эхокардиографии, по сравнению с предыдущим обследование без существенной динамики, ФВ ЛЖ — 51%, полости желудочков не расширены.
Общий анализ крови и мочи без патологии. В биохимических анализах крови по сравнению с предыдущей госпитализацией обнаружены повышение тропонина I — 0,90 нг/мл (< 0,5), гипокалиемия — 3,2 ммоль/л (3,5–5,2 ммоль/л), снижение общего белка — 51,0 г/л (55,0–75,0), альбумин — 21 г/л (25,0–39,0), повышение билирубина общ. — 43,0 мкмоль/л (1,7–21,0), билирубин прямой — 6,0 мкмоль\л (0,0–5,50), более значительное увеличение АлАТ — 78 мкмоль/л (7–41) и АсАТ — 58 мкмоль/л (10–38); повышение гамма-глутамилтранспептидазы (ГГТ) — 76 Ед/л и глюкозы — 6,4 ммоль/л (3,9–6,1); NT-pro-DNP — 450 пг/мл (< 125).
Проводилась дифференциальная диагностика с острым коронарным синдромом.
Консультация невролога: симметричная полиневропатия (токсическая?).
По-прежнему генез тяжёлой сердечной недостаточности с длительной ремиссией был неясен, однако присоединение неврологической симптоматики (симметричная полинейропатия в отсутствии сахарного диабета и других причин её возникновения) и некоторые особенности поведения больной позволили заподозрить хроническое злоупотребление алкоголем, которое пациентка категорически отрицала. После беседы с мужем выяснилось, что больная в течение 20 лет злоупотребляет алкоголем (ежедневно выпивала 300-500 мл коньяка), госпитализации по поводу выраженной сердечной недостаточности были обусловлены тяжёлыми алкогольными эксцессами (запои).
Вместе с тем традиционное лечение ХСН в сочетании с дезинтоксикацией, препаратами калия, магния, витаминами группы В вновь достаточно быстро привели к уменьшению признаков декомпенсации, в лёгких хрипы отсутствуют, число дыханий — 17 в минуту, тоны сердца ритмичные, сохранялась постоянная тахикардия 88–94 уд./мин. (100 мг метопролола сукцинат), исчезли отёки нижних конечностей. Тропонин нормализовался на 3-и сутки.
От консультации нарколога и психиатра категорически отказалась, была выписана домой в удовлетворительном состоянии с рекомендациями полностью отказаться от приёма алкоголя.
Обсуждение
Представленный случай демонстрирует позднюю диагностику поражения сердечно-сосудистой системы у пациентки с хронической алкогольной интоксикацией.
При первой госпитализации пациентки с выраженными проявлениями сердечной недостаточности (со слов больной, впервые) не было выявлено какого-либо серьёзного заболевания сердца, кроме умеренной гипертрофии левого желудочка, которая могла быть объяснена плохо леченной АГ. Известно, что артериальная гипертензия — одна из наиболее распространённых патологий сердечно-сосудистой системы у больных хронической алкогольной интоксикацией. Достаточно быстрое обратное развитие проявлений сердечной недостаточности и полное их отсутствие в течение 1 года (больная активно работала и много путешествовала в страны с жарким климатом) характерно для алкогольного поражения сердца. Проводилась дифференциальная диагностика с острым коронарным синдромом. Боли в груди, повышение уровня тропонина во вторую госпитализацию, вероятно, являлись отражением повреждения миокарда из-за токсического действия этанола, наличия тахиаритмий и сердечной недостаточности, симпатоадреналовой активации вследствие предшествующего алкогольного эксцесса. Кратковременные подъёмы тропонинов при СН связаны с нарушением сократимости миокарда и коррелируют с тяжестью СН и прогнозом [9].
Несмотря на выраженные проявления сердечной недостаточности, расширения желудочков не отмечалось. При далеко зашедшей АКМП как правило, развивается выраженная дилатация полостей сердца.
У пациентки сердечная недостаточность с сохранённой фракцией выброса (СНсФВ), которая является распространённым, но трудно диагностируемым заболеванием. СНсФВ ассоциирована с коморбидностью, поэтому её симптомы не всегда специфичны, что часто обусловливает длительный диагностический поиск и невозможность лечения основного заболевания и профилактики его осложнений. Ведущими морфофункциональными нарушениями при СНсФВ являются интерстициальный фиброз, окислительный стресс, эндотелиальная дисфункция, нарушение микроциркуляции, которые в итоге формируют ремоделирование ЛЖ, его систолическую и диастолическую дисфункцию [10][11].
Подтверждением СНсФВ у больной являются данные ЭхоКГ: увеличение ИКСО ЛП до 34 мл/м2, увеличение индекса массы миокарда ЛЖ (ИММЛЖ) до 122 г/м2, наличие диастоличсекой дисфункции по типу замедления релаксации.
Тяжёлые аритмии в период обострения заболевания возникали только при алкогольных эксцессах и в период абстиненции (со слов мужа), отражая повышенное высвобождение катехоламинов и дефицит электролитов (калий крови — 3,2 ммоль/л). Пароксизмы ФП («синдром праздничного сердца») с высоким ЧСС (до 190 уд./мин.) характерны для алкогольного сердца из-за укорочения рефрактерного периода правого предсердия и возникновения эффекта «сверхпроводимости» на желудочки. Такая «сверхпроводимость» возможна также при тиреотоксикозе, синдроме WPW, которые были исключены. Частая политопная желудочковая экстрасистолия, включая «пробежки» желудочковой тахикардии (регистрировались при ФП), усугубляла нарушения гемодинамики и являлась риском внезапной смерти. Постоянно существующая синусовая тахикардия отражает вегетативный дисбаланс с преобладанием тонуса симпатической нервной системы.
В первую госпитализацию тяжёлый гипертонический криз с выраженной вегетативной симптоматикой был проявлением абстинентного синдрома вследствие выброса дофамина («дофаминовый криз»). Известно, что частота и выраженность кризов при алкогольной зависимости очень индивидуальна и может значительно различаться при сходном алкогольном анамнезе и возрасте пациентов [2].
Сама пациентка связывала его с прекращением (по совету гинеколога) менопаузальной гормональной терапии, которую она получала в течение 4-х лет из-за «выраженных приливов, потливости, нарушений сна». Весьма вероятно, что описанные симптомы усугублялись алкогольной интоксикацией.
Своевременную диагностику затрудняло то, что пациентка не находилась под динамическим врачебным наблюдении, скрывала факт злоупотребления алкоголем. Подозрение о происхождении кардиальных симптомов возникли лишь при появлении типичных для алкоголизма неврологических симптомов, отражая алкогольную полиневропатию, а изменение лабораторных показателей, характеризующих функцию печени (АсАТ, АлАТ, ГТТ) относили к застойным явлениям. Между тем, стигмы хронической алкоголизации в виде расширения сосудистого рисунка на лице, гиперемии ладоней («пальмарная эритема») у больной присутствовали.
Таким образом, в результате длительного злоупотребления алкоголем у пациентки присутствуют признаки полиорганного поражения: сердца, периферической нервной системы, печени (жировой гепатоз).
Заключение
Поражение сердечно-сосудистой системы нередко встречается при острой и хронической алкогольной интоксикации и имеет разнообразные клинические проявления, в том числе в виде сердечной недостаточности и аритмий. Риск развития ССЗ и уровень смертности, безусловно, зависят от количества и длительности потребления алкоголя. Однако факт злоупотребления алкоголем как причина выявляется достаточно поздно, что приводит к неадекватному ведению пациентов, высокому риску осложнений и неблагоприятным исходам. Смертность при алкогольном поражении сердца может быть связана с прогрессированием сердечной недостаточности и злокачественными аритмиями.
Воздержание от алкоголя позволяет значительно улучшить прогноз.
Тактику ведения следует разрабатывать совместно командой врачей (кардиолог, терапевт, психиатр, нарколог и специалисты по сопутствующей патологии) с коррекцией всех нарушений, вызванных алкоголем, включая недостаточное питание, нарушения витаминного и электролитного баланса с учётом индивидуальных особенностей течения заболевания.
Финансирование. Исследование не имело спонсорской поддержки.
Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов.
Список литературы
1. Day E, Rudd JHF. Alcohol use disorders and the heart. Addiction. 2019;114(9):1670-1678. DOI: 10.1111/add.14703.
2. Кобалава Ж.Д., Лазарев П.В., Гончаров А.С. Современный взгляд на проблемы патогенеза, диагностики и лечения алкогольной кардиомиопатии. Российский кардиологический журнал. 2019;(11):164-172. DOI: 10.15829/1560-4071-2019-11-164-172
3. Fernández-Solà J. The Effects of Ethanol on the Heart: Alcoholic Cardiomyopathy. Nutrients. 2020;12(2):572. DOI: 10.3390/nu12020572.
4. Sutanto H, Cluitmans MJM, Dobrev D, Volders PGA, Bébarová M, Heijman J. Acute effects of alcohol on cardiac electrophysiology and arrhythmogenesis: Insights from multiscale in silico analyses. J Mol Cell Cardiol. 2020;146:69-83. DOI: 10.1016/j.yjmcc.2020.07.007.
5. Piano MR. Alcohol’s Effects on the Cardiovascular System. Alcohol Res. 2017;38(2):219-241. PMID: 28988575; PMCID: PMC5513687.
6. Пауков В. С., Кириллов Ю. А., Ерохин Ю. А., Чернов И. А. Изменения сердца и сосудов в пато- и морфогенезе алкогольной болезни. Кардиоваскулярная терапия и профилактика. 2020;19(5):2436. DOI: 10.15829/1728-8800-2020-2436.
7. Kim YG, Han KD, Choi JI, Boo KY, Kim DY, Lee KN, et al. Frequent drinking is a more important risk factor for new-onset atrial fibrillation than binge drinking: a nationwide population-based study. Europace. 2020;22(2):216-224. DOI: 10.1093/europace/euz256.
8. Brunner S, Winter R, Werzer C, von Stülpnagel L, Clasen I, Hameder A, et al. Impact of acute ethanol intake on cardiac autonomic regulation. Sci Rep. 2021;11(1):13255. DOI: 10.1038/s41598-021-92767-y.
9. Дупляков Д.В., Чаулин А.М. Мутации сердечных тропонинов, ассоциированные с кардиомиопатиями. Кардиология: новости, мнения, обучение. 2019;7(3):8–17. DOI: 10.24411/2309-1908-2019-13001.
10. Almeida P, Rodrigues J, Lourenço P, Maciel MJ, Bettencourt P. Left atrial volume index is critical for the diagnosis of heart failure with preserved ejection fraction. J Cardiovasc Med (Hagerstown). 2018;19(6):304-309. DOI: 10.2459/JCM.0000000000000651.
11. Драпкина О. М., Джиоева О. Н. Современные эхокардиографические критерии сердечной недостаточности с сохраненной фракцией выброса: не только диастолическая дисфункция. Кардиоваскулярная терапия и профилактика. 2020;19(2):2454. DOI: 10.15829/1728-8800-2020-2454
12. Шкарин Вл.В., Горбунова М.Л., Пегелау Т.К., Попова Н.А., Власова Т.В., Белькин Ю.А., и др. Тактика ведения больных с сердечными аритмиями. Учебное пособие. 2017. eLIBRARY ID: 32417871
Об авторах
Е. И. ТарловскаяРоссия
Тарловская Екатерина Иосифовна, д.м.н., профессор, зав. кафедрой, кафедра терапии и кардиологии
Нижний Новгород
Е. В. Соловьёва
Россия
Соловьева Елена Витальевна, к.м.н., доцент, кафедра терапии и кардиологии
Нижний Новгород
Н. А. Попова
Россия
Попова Наталия Алексеевна, к.м.н., доцент, кафедра терапии и кардиологии
Нижний Новгород
Т. В. Власова
Россия
Власова Татьяна Владимировна, к.м.н., доцент, кафедра терапии и кардиологии
Нижний Новгород
М. Л. Горбунова
Россия
Горбунова Марина Леонидовна, к.м.н., доцент, врач кардиолог
Нижний Новгород
Н. В. Идабаева
Россия
Идабаева Наталия Валериановна, врач кардиолог
Нижний Новгород
Ю. А. Почукалина
Россия
Почукалина Юлия Андреевна, клинический ординатор, кафедра терапии и кардиологии
Нижний Новгород
Дополнительные файлы
Рецензия
Для цитирования:
Тарловская Е.И., Соловьёва Е.В., Попова Н.А., Власова Т.В., Горбунова М.Л., Идабаева Н.В., Почукалина Ю.А. Ошибки диагностики и сложности ведения пациентов с алкогольным поражением сердца. Южно-Российский журнал терапевтической практики. 2022;3(2):100-106. https://doi.org/10.21886/2712-8156-2022-3-2-100-106
For citation:
Tarlovskaya E.I., Solovyova E.V., Popova N.A., Vlasova T.V., Gorbunova M.L., Idabaeva N.V., Pochukalina Yu.A. A clinical case of arrhythmogenic right ventricular dysplasia (ADP). South Russian Journal of Therapeutic Practice. 2022;3(2):100-106. (In Russ.) https://doi.org/10.21886/2712-8156-2022-3-2-100-106
JATS XML

























