Перейти к:
Аутоиммунные энцефалиты: взгляд невролога (сложные вопросы диагностики)
https://doi.org/10.21886/2712-8156-2025-6-1-19-26
Аннотация
Аутоиммунные энцефалиты (АИЭ) представляют собой неинфекционные иммуноопосредованные воспалительные заболевания паренхимы мозга с частым поражением коркового или глубокого серого вещества с вовлечением или без вовлечения белого вещества головного мозга, мозговых оболочек или спинного мозга. Наиболее частыми клиническими синдромами АИЭ являются расстройства психики, поведения, когнитивных и вегетативных функций, двигательные нарушения, а также эпилептические приступы. Диагностику АИЭ может затруднять изолированная представленность психопатологической галлюцинаторно-бредовой и эмоционально-аффективной симптоматики, что может имитировать дебют идиопатического психического расстройства и требует определённой настороженности и повышенного внимания к данным анамнеза и оценке неврологического статуса. МРТ-паттерн лимбического энцефалита с одно- или двусторонним поражением медиальных отделов височных долей является типичным для АИЭ, однако возможны как нормальная МРТ головного и/или спинного мозга, так и вовлечение самых различных отделов головного мозга при разных подтипах АИЭ. Необходимо учитывать вероятность не только рецидивирующего течения АИЭ, но и возможность развития перекрывающихся синдромов АИЭ и других аутоиммунных расстройств, включая демиелинизирующие заболевания: рассеянный склероз, расстройства спектра оптиконейромиелита или заболевания, ассоциированные с антителами к миелин-олигодендроцитарному гликопротеину, — что требует более длительного наблюдения из-за риска рецидива аутоиммунных заболеваний.
Ключевые слова
Для цитирования:
Сорокин Ю.Н., Сорокина Е.Ю. Аутоиммунные энцефалиты: взгляд невролога (сложные вопросы диагностики). Южно-Российский журнал терапевтической практики. 2025;6(1):19-26. https://doi.org/10.21886/2712-8156-2025-6-1-19-26
For citation:
Sorokin Yu.N., Sorokina E.Yu. Autoimmune encephalitis: neurologist’s view (complex questions of diagnostics). South Russian Journal of Therapeutic Practice. 2025;6(1):19-26. (In Russ.) https://doi.org/10.21886/2712-8156-2025-6-1-19-26
Аутоиммунные энцефалиты: причины развития и классификация
Аутоиммунные энцефалиты (АИЭ) представляют собой неинфекционные иммуноопосредованные воспалительные заболевания паренхимы мозга с частым поражением коркового или глубокого серого вещества с вовлечением или без вовлечения белого вещества, мозговых оболочек или спинного мозга. При этом воспалительный процесс является аутоиммунным и развивается вследствие взаимодействия образовавшихся антител с вне- и внутриклеточными невральными структурами, выступающими в роли антигенов [1]. В настоящее время для коммерческого тестирования в мире доступны 40 нейрональных аутоантител [2], в России — около 20 [3].
В проведённом в Китае многоцентровом ретроспективном исследовании, в котором за 5 лет было зарегистрировано 778 случаев определённого АИЭ, основными подтипами АИЭ были энцефалиты с антителами к NMDAR (61%), LGI1 (21%), GABABR (11%) и CRASPR (3%) антигенам [4].
Антитела могут образовываться вследствие презентации антигенов злокачественного новообразования или инфекционных агентов (например, после энцефалита, вызванного вирусом простого герпеса, почти у трети пациентов развивается АИЭ, при этом у одной половины с NMDAR-антителами, у другой — с антителами против неизвестных нейронных эпитопов), а также идиопатически или при применении новых методов лечения рака (ингибиторов иммунных контрольных точек или других иммуномодулирующих средств). В связи с этим этиологическая классификация выделяет паранеопластические, пост(пара)инфекционные, идиопатические и ятрогенные АИЭ (табл. 1), а серологическая — АИЭ с антителами к внутриклеточным антигенам (классические онконейрональные антитела), поверхностным антигенам и другим антигенам с высокой или низкой клинической значимостью и серонегативные. С учётом клинических и нейровизуализационных данных для практического применения удобной также является анатомическая классификация АИЭ [2].
Таблица / Table 1
Классификация аутоиммунных энцефалитов [2]
Classification of autoimmune encephalitis [2]
Этиологическая классификация |
Паранеопластический энцефалит |
Пост(пара)инфекционный энцефалит |
Идиопатический энцефалит |
Ятрогенный энцефалит |
Серологическая классификация |
Энцефалит с антителами к внутриклеточным антигенам (классические онконейрональные антитела — Hu, Ri, Yo, CV2/CRMP5, Ма1/Ma2, Tr) |
Энцефалит с антителами к поверхностным антигенам и другим антигенам с высокой клинической значимостью (NMDAR, AMPAR, LGI1, CASPR2, GABAAR, GABABR, DPPX, GlyR, AQP4, MOG, GFAP) |
Энцефалит с антителами к поверхностным антигенам с низкой клинической значимостью (VGKC, VGCC) |
Серонегативный аутоиммунный энцефалит |
Анатомическая классификация |
Лимбический энцефалит |
Корковый/подкорковый энцефалит |
Стриарный энцефалит |
Диэнцефальный энцефалит |
Стволовой энцефалит |
Мозжечковый энцефалит |
Энцефаломиелит |
Менингоэнцефалит |
Комбинированные формы |
Особенности клинических проявлений аутоиммунных энцефалитов
В клинической картине АИЭ нет чётко выраженного синдрома, при этом спектр клинических проявлений достаточно широк, с очень изменчивыми и малоспецифичными неврологическими синдромами. Диагностические критерии возможного АИЭ акцентируют внимание на подостром начале и быстром прогрессировании (менее чем за 3 месяца) психопатологической симптоматики, нарушения сознания и когнитивных функций на фоне впервые выявленных признаков очагового поражения головного мозга (чаще — в виде двигательных расстройств) и эпилептических приступов при исключении альтернативных причин. Лабораторные данные включают плеоцитоз в ликворе и гиперденсивные Т2/FLAIR-изменения в медиальных отделах височных долей или мультифокальное поражение серого и/или белого вещества головного мозга при магнитно-резонансной томографии (МРТ). Подтверждение диагноза требует патоморфологического или серологического доказательства аутоиммунного патологического процесса, четко ассоциированного с энцефалитом [1][5].
В целом основные клинические симптомы заболевания можно представить на примере обследования 242 пациентов с наиболее распространёнными типами АИЭ: NMDAR-, LGI1- и GABABR-энцефалитом (табл. 2). Вегетативная дисфункция проявлялась (в порядке убывания частоты) нарушением моторики желудочно-кишечного тракта, синусовой тахикардией, синдромом центральной гиповентиляции, недержанием или задержкой мочи, лабильностью артериального давления, ортостатической гипотензией, брадикардией, повышенным слюноотделением, гипергидрозом, полиурией, центральной гипертермией, предсердной или желудочковой тахикардией, кардиальной асистолией. При этом у 24% пациентов на МРТ обнаружены гиперденсивные изменения в височных долях [6].
Таблица / Table 2
Клиническая характеристика аутоиммунных энцефалитов [6]
Clinical characteristics of autoimmune encephalitis [6]
Клинический синдром Clinical syndrom | NMDAR (n=147) | LGI1 (n=48) | GABABR (n=47) | Все типы All types |
Когнитивные нарушения Cognitive problems | 74% | 69% | 91% | 77% |
Расстройства психики и поведения Mental and behavior changes | 82% | 60% | 85% | 79% |
Эпилептические приступы Seizures | 65% | 77% | 83% | 71% |
Вегетативная дисфункция Autonomic symptoms | 55% | 29% | 76% | 54% |
Нарушения речи Speech problems | 48% | 15% | 45% | 40% |
Типичным вариантом АИЭ является лимбический энцефалит, который ассоциируется с различными типами антител: к нейрексин-3α, Hu, CRMP5/CV2, Ma2, NMDAR, AMPAR, LGI1, CASPR2, GAD65, GABABR, DPPX, mGluR5 и AK5. Возможен и вариант серонегативного лимбического энцефалита. АИЭ с другой локализацией очагов поражения будут проявляться иными неврологическими синдромами.
Корковый/подкорковый энцефалит проявляется когнитивными нарушениями и эпилептическими приступами и ассоциируется со следующими типами антител: PCA-2 (MAP1b), NMDAR, GABAA/BR, DPPX и MOG.
Для стриарного энцефалита характерны экстрапирамидные двигательные расстройства (гиперкинетические (хорея, баллизм, дистония, дискинезии) или гипокинетические (вариабельные ассоциации акинезии/брадикинезии, тремора покоя и ригидности)) в сочетании с психопатологическими симптомами и антителами CRMP5/CV2, D2R, NMDAR, LGI1 и PDЕ10A.
Диэнцефальный энцефалит проявляется вегетативными нарушениями, брадикинезией, снижением концентрации внимания, аффективным уплощением, гиперсомнией и гиперфагией из-за поражения гипоталамуса и связан с антителами Ma1/2, IgLON5, DPPX и AQP4.
Стволовой энцефалит характеризуется дисфункцией черепных нервов, двигательными нарушениями, сенсорной атаксией и характерен для АИЭ с антителами Ri, Hu, Ма1/2, PCA-2 (MAP1b), KLHL11, IgLON5, NMDAR, GABAA/BR, DPPX, AQP4, MOG и GQ1b.
При мозжечковом энцефалите (подострая паранеопластическая мозжечковая дегенерация) мозжечковый синдром включает головокружение, осциллопсии, дисметрию и атаксию и ассоциируется с антителами Yo, Hu, Ri, Tr, CASPR2, KLHL11, NIF, mGluR1, GAD65 и VGCC.
Менингоэнцефалит проявляется когнитивными нарушениями и эпилептическими приступами с вовлечением оболочек мозга, может ассоциироваться с GFAP-антителами или быть серонегативным АИЭ. В целом эпилептические приступы могут наблюдаться при лимбической, корковой и менингоэнцефалитической формах АИЭ, составляют часть ядра клинической картины острой фазы АИЭ, чаще ассоциируются с антителами против внеклеточных антигенов нейронов и характеризуются множественной семиологией приступов [7][8].
Энцефаломиелит характеризуется двигательными расстройствами (включая прогрессирующий энцефаломиелит с ригидностью и миоклонусом и синдром ригидного человека), спинальными сенсорными и тазовыми нарушениями или оптикоспинальным синдромом и ассоциируется с антителами к амфифизину, GAD65, GlyR, PCA-2 (MAP1B), GABAA/BR, DPPX, CRMP5/CV2, AQP4 и MOG [9].
Относительно патогномоничными проявлениями АИЭ можно считать развитие психоза при NMDAR-, AMPAR- и GABAA/BR-энцефалитах и GFAP-астроцитопатии, нейромиотонию и фасцикуляции при CASPR2-энцефалите, диарею и потерю веса при DPPX-энцефалите и фациобрахиальные дистонические приступы при LGI1-энцефалите [5].
Сложности клинической диагностики аутоиммунных энцефалитов
Особые затруднения с постановкой диагноза «АИЭ» возникают при изолированном или превалирующем развитии психопатологической галлюцинаторно-бредовой и эмоционально-аффективной симптоматики, которая является одним из наиболее частых клинических синдромов АИЭ вообще, может имитировать дебют идиопатического психического расстройства и быть причиной госпитализации в психиатрическую клинику [10][11].
Для диагностики таких «стертых» форм NMDAR-энцефалита необходимо обращать внимание на особенности клинической симптоматики, нехарактерные для стереотипного развития психического расстройства. Острое или подострое развитие заболевания, продромальный период в виде «гриппоподобного» состояния, отсутствие психотических эпизодов в анамнезе, поздний возраст их начала, кататония, грубые нарушения памяти, дискинезии, гипонатриемия, волнообразное течение, отсутствие ответа на проводимую терапию нейролептиками или побочные эффекты такого лечения в виде злокачественного нейролептического синдрома — всё это должно настораживать в отношении дебюта АИЭ и побуждать к исследованию сыворотки крови и/или ликвора на наличие нейрональных антител [12].
Описаны три клинических фенотипа психопатологической симптоматики при АИЭ у детей с различным ответом на иммунотерапию: 1) «классический» — с кататоническим или ступорозным состоянием длительностью менее 60 дней и хорошим ответом на агрессивную иммунотерапию; 2) с доминированием галлюцинаторно-бредовой и эмоционально-аффективной симптоматики без клинических симптомов кататонии и хорошим ответом на 1-ю линию терапии; 3) с доминированием кататонической симптоматики более 60 дней и резистентностью к любой линии терапии [13].
Особенности лабораторной диагностики аутоиммунных энцефалитов
В результате проведения МРТ головного мозга в части случаев АИЭ выявляются относительно неспецифические поражения, в других случаях обнаруживаются характерные паттерны нейровизуализации. В связи с этим в зависимости от поражения головного мозга на МРТ испанские авторы предложили разделить АИЭ на три группы: с нормальной МРТ головного и/или спинного мозга, с паттерном лимбического энцефалита и с другими паттернами поражения ЦНС. Отдельно рассматриваются паранеопластический энцефалит и АИЭ, ассоциированные с новыми методами лечения рака [5].
Нормальная МРТ головного и/или спинного мозга часто наблюдается при синдроме ригидного человека с его различными фенотипами: классического варианта клинической картины, клиники прогрессирующего энцефаломиелита с синдромом ригидности и миоклонуса и с паранеопластической картиной, при анти-IgLON5 болезни — новой формы таупатии, при которой сочетаются механизмы аутоиммунных нарушений и нейродегенерации, в острой стадии NMDAR-энцефалита (≥50% случаев) и LG1-энцефалита (25% случаев) [5][14].
В целом при NMDAR-энцефалите возможны самые различные паттерны МРТ-поражений. Наиболее характерными являются неспецифические гиперинтенсивные поражения белого вещества (40% случаев), преимущественно лобной (рис. 1), реже височной и теменной долей. Также наблюдаются изменения коркового серого вещества, поражения глубоких структур серого вещества (базальные ганглии, гиппокамп, гипоталамус), поражения ствола мозга или мозжечка. При этом в острой стадии вовлечение гиппокампа отмечается достаточно редко, в отличие от лимбического АИЭ — при LG1-энцефалите односторонняя или двусторонняя T2/FLAIR-гиперинтенсивность медиальных отделов височных долей выявляется в 70% случаев (рис. 1) [14].
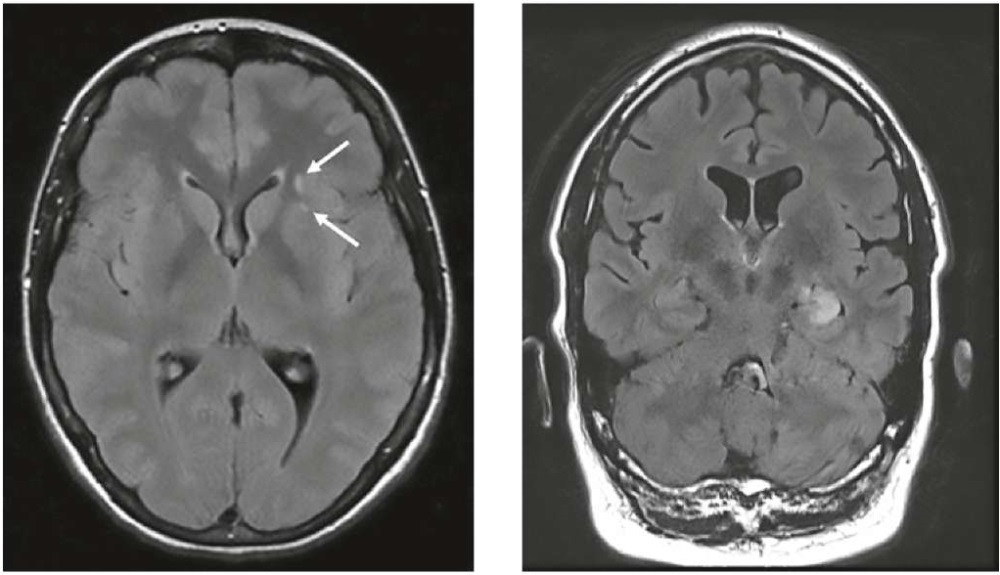
Рисунок 1. Слева — два небольших неспецифических T2/FLAIR-гиперинтенсивных очага в левой лобной доле при NMDAR-энцефалите; справа — T2/FLAIR-гиперинтенсивность в медиальных отделах левой височной доли при LG1-энцефалите в стадии лимбического энцефалита [14].
Figure 1. Left — two small non-specific T2/FLAIR-hyperintense lesions in the left frontal lobe in NMDAR-encephalitis; right — T2/FLAIR-hyperintensity in the left medial temporal lobe in LG1-encephalitis at the stage of limbic encephalitis [14].
Особо специфичный МРТ-паттерн периваскулярного поражения выявляется при аутоиммунной астроцитопатии с GFAP-антителами в виде характерных радиальных и ламинарных T2/FLAIR-гиперинтенсивных очагов поражения с лептоменингеальным и линейным периваскулярным контрастным усилением в белом веществе перпендикулярно желудочкам мозга (рис. 2) [5][15].
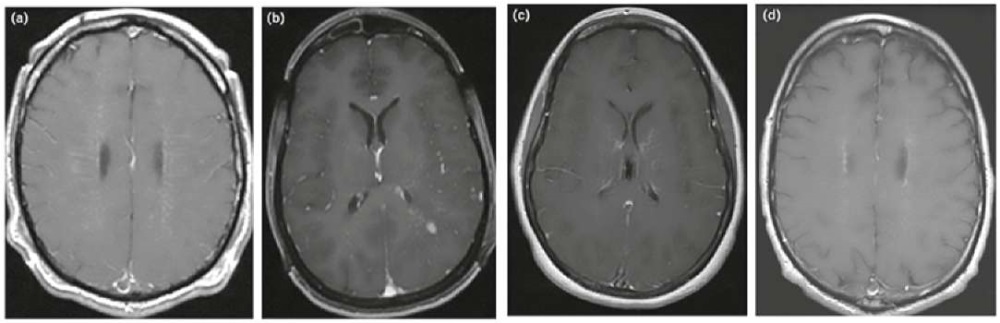
Рисунок 2. Паттерны контрастного усиления сигнала при аутоиммунной GFAP-астроцитопатии: (a) радиальный перивентрикулярный, (b) лептоменингеальный и точечный, (c) извилистый/змеевидный, (d) периэпендимальный [15].
Figure 2. Patterns of contrast enhancement in autoimmune GFAP-astrocytopathy: (a) radial periventricular, (b) leptomeningeal and punctate, (c) serpiginous, (d) periependymal [15].
Исследование ликвора является вторым шагом в обследовании после МРТ головного мозга. Наличие воспалительных изменений при этом подтверждаются появлением цитоза (обычно невысокого, десятки клеток, меньше, чем при инфекционных энцефалитах; редко — 200–900 клеток) и увеличением содержания белка, в некоторых случаях отмечаются повышенный индекс IgG и/или скорость синтеза IgG и положительные интратекальные олигоклональные полосы (при их отсутствии в сыворотке).
Ликвор более чувствителен для тестирования антител NMDAR и GFAP, а сыворотка крови — для онконейрональных антител и антител LGI1 и AQP4. При этом возможно выявление у одного и того же пациента более одного типа антител или выявление антител при отсутствии воспалительных изменений в ликворе. Исследование крови и ликвора необходимо также для исключения других патологических состояний из круга дифференциальной диагностики.
С учётом того, что неврологические симптомы могут нередко развиваться раньше выявления злокачественного новообразования, которое может обнаруживаться даже после выздоровления от энцефалита, необходимо проведение стандартного онкопоиска, а определение паранеопластических антител без выявления первичной опухоли требует повторения онкопоиска в динамике. При отсутствии у пациента опухоли, по данным позитронно-эмиссионной томографии всего тела, необходимо динамическое наблюдение с повторением онкопоиска каждые 3 месяца до выявления новообразования с акцентом на область, с которой потенциально ассоциированы выявленные у пациента аутоантитела.
Особенности течения аутоиммунных энцефалитов
АИЭ характеризуются склонностью к рецидивированию, при этом общая частота рецидивов NMDAR-, LGI1- и GABABR-энцефалитов в течение двух лет после острой фазы заболевания составляет 26%. Рецидивы обычно (67% случаев) менее тяжёлые, чем первоначальный эпизод АИЭ. Повышенный риск рецидива имеют пациенты, получившие иммунотерапию в острой фазе заболевания с задержкой. При LGI1-энцефалите вероятность рецидива коррелирует также с концентрацией титра антител в остром периоде [16][17].
В то время как злокачественные новообразования и герпетический энцефалит являются двумя подтверждёнными иммунологическими триггерами NMDAR-энцефалита, в последнее время появляется всё больше описаний случаев наложения проявлений NMDAR-энцефалита и рассеянного склероза, когда после перенесённого NMDAR-энцефалита почти в 12% случаев развивается клиническая симптоматика, типичная для РС, в сочетании с изменениями на МРТ, соответствующими критериям диссеминации в пространстве и во времени. При таком синдроме перекрытия накопление T2-очагов за 5 лет оказывается более значительным (1,32 в год) по сравнению со случаями рецидивов при изолированных NMDAR-энцефалите (0,01 в год; p<0,001) или ремиттирующем рассеянном склерозе (0,48 в год; p<0,001), в связи с чем предлагается проводить контрольную МРТ через 12–24 месяца после перенесённого NMDA-энцефалита для выявления клинически бессимптомных демиелинизирующих поражений [14][18].
Описан случай развития лимбического АИЭ с антителами против неизвестных нейронных эпитопов через 5 месяцев после перенесённого энцефалита, вызванного вирусом опоясывающего герпеса, а ещё через 1 год у этой же пациентки появились клинические симптомы и радиологические признаки демиелинизирующего поражения головного и спинного мозга и был констатирован диагноз «Рассеянный склероз» [19].
Также выявлены случаи NMDAR-энцефалита с одновременным сосуществованием расстройства спектра оптиконейромиелита (в 5% случаев) или заболевания, ассоциированного с антителами к миелин-олигодендроцитарному гликопротеину (MOГ). При этом на МРТ выявляются типичные характеристики этих состояний: прехиазмальный двусторонний неврит зрительного нерва, поражение спинного мозга в виде продольно-распространённого поперечного миелита, изменения в стволе мозга и мультифокальные поражения белого вещества головного мозга. Предполагается, что указанные перекрывающиеся синдромы нуждаются в долгосрочной иммуносупрессивной терапии с использованием препаратов второй линии уже на ранней стадии в соответствии с текущими рекомендациями по лечению расстройств спектра оптиконейромиелита или МОГ-ассоциированных заболеваний. В то же время возможно сосуществование NMDAR-энцефалита и с другими аутоиммунными расстройствами, включая синдром Шегрена, системную красную волчанку, тиреоидит Хашимото и миастению [14][20][21].
Заключение
Таким образом, диагностику АИЭ может затруднять изолированная представленность психопатологической галлюцинаторно-бредовой и эмоционально-аффективной симптоматики, что может имитировать дебют идиопатического психического расстройства и требует определенной настороженности и повышенного внимания к данным анамнеза и оценке неврологического статуса.
Необходимо учитывать вероятность не только рецидивирующего течения АИЭ, но и возможность развития перекрывающихся синдромов АИЭ и других аутоиммунных расстройств, включая демиелинизирующие заболевания, такие как рассеянный склероз, расстройства спектра оптиконейромиелита или МОГ-ассоциированные заболевания, что требует более длительного наблюдения из-за риска рецидива аутоиммунных заболеваний.
Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов.
Финансирование. Исследование не имело спонсорской поддержки.
Список литературы
1. Graus F., Titulaer M.J, Balu R. Benseler S., Bien Ch.G., Cellucci Т. et al. A clinical approach to diagnosis of autoimmune encephalitis. Lancet Neurol. 2016;15(04):391-404. DOI: 10.1016/S1474-4422(15)00401-9
2. Abboud H, Probasco JC, Irani S, Ances B, Benavides DR, Bradshaw M, et al. Autoimmune encephalitis: proposed best practice recommendations for diagnosis and acute management. J Neurol Neurosurg Psychiatry. 2021;92(7):757-768. DOI: 10.1136/jnnp-2020-325300
3. Полонский Е.Л., Скулябин Д.И., Лапин С.В., Красаков И.В., Тихомирова О.В., Назаров В.Д. и др. Полиморфизм аутоиммунного энцефалита. Анналы клинической и экспериментальной неврологии. 2019;13(2):79-91. DOI: 10.25692/ACEN.2019.2.9
4. Shan W, Yang H, Wang Q. Neuronal Surface Antibody-Medicated Autoimmune Encephalitis (Limbic Encephalitis) in China: A Multiple-Center, Retrospective Study. Front Immunol. 2021;12:621599. DOI: 10.3389/fimmu.2021.621599
5. Arbizu J, Gállego Pérez-Larraya J, Hilario A, Gómez Grande A, Rubí S, Camacho V; et al. Update on the diagnosis of encephalitis. Rev Esp Med Nucl Imagen Mol (Engl Ed). 2022;41(4):247-257. DOI: 10.1016/j.remnie.2022.05.003
6. Yang M, Lian Y. Clinical Features and Early Recognition of 242 Cases of Autoimmune Encephalitis. Front Neurol. 2022;12:803752. DOI: 10.3389/fneur.2021.803752
7. Сорокин Ю.Н., Сорокина E.Ю. Особенности эпилептических приступов при аутоиммунном энцефалите. Университетская клиника. 2022;(S2):297–299.
8. Евтушенко С.К., Сорокин Ю.Н. Эпилептические проявления аутоиммунных энцефалитов. Российский неврологический журнал. 2023;28(4):81-86. DOI: 10.30629/2658-7947-2023-28-4-81-86
9. Исаева Н.В., Прокопенко С.В., Родиков М.В., Аброськина М.В., Ондар В.С., Субочева С.А., и др. Синдром ригидного человека: особенности клинического течения. Журнал неврологии и психиатрии им. С.С. Корсакова. 2019;119(6):96‑100. DOI: 10.17116/jnevro201911906196
10. Хорева М.А., Серикова И.Ю., Смагина И.В., Голенко А.А., Смирнов К.В., Завьялов А.Е., и др. Клинический случай энцефалита с антителами к NMDA-рецепторам на фоне новой коронавирусной инфекции (COVID-19). Российский неврологический журнал. 2022;27(1):106-112. DOI: 10.30629/2658-7947-2022-27-1-106-112
11. Панченко Н.И., Шулешова Н.В., Руденко Д.И., Скулябин Д.И., Колчев С.А., Перфильев С.В., и др. Аутоиммунный анти-NMDA-энцефалит, ассоциированный с новой коронавирусной инфекцией COVID-19. Российский неврологический журнал. 2023;28(4):60-67. DOI: 10.30629/2658-7947-2023-28-4-60-67
12. Мурашко А.А. Мимикрия: анти-NMDA рецепторный энцефалит и психические расстройства. Социальная и клиническая психиатрия. 2022;32(4):59-67. eLIBRARY ID: 50489610 EDN: LJESPJ
13. DeSena AD, Greenberg BM, Graves D. Three phenotypes of anti-N-methyl-D-aspartate receptor antibody encephalitis in children: prevalence of symptoms and prognosis. Pediatr Neurol. 2014;51(4):542-549. DOI: 10.1016/j.pediatrneurol.2014.04.030
14. Hartung TJ, Bartels F, Kuchling J, Krohn S, Leidel J, Mantwill M, et al. MRI findings in autoimmune encephalitis. Rev Neurol (Paris). 2024;180(9):895-907. DOI: 10.1016/j.neurol.2024.08.006
15. Kunchok A, Zekeridou A, McKeon A. Autoimmune glial fibrillary acidic protein astrocytopathy. Curr Opin Neurol. 2019;32(3):452-458. DOI: 10.1097/WCO.0000000000000676
16. Titulaer MJ, McCracken L, Gabilondo I, Armangué T, Glaser C, Iizuka T,et al. Treatment and prognostic factors for long-term outcome in patients with anti-NMDA receptor encephalitis: an observational cohort study. Lancet Neurol. 2013;12(2):157-165. DOI: 10.1016/S1474-4422(12)70310-1
17. Zhong R, Chen Q, Zhang X, Zhang H, Lin W. Relapses of Anti-NMDAR, Anti-GABABR and Anti-LGI1 Encephalitis: A Retrospective Cohort Study. Front Immunol. 2022;13:918396. DOI: 10.3389/fimmu.2022.918396
18. Yang B, Yu N. Glucocorticoid-dependent multiple sclerosis overlapping anti-NMDA receptor encephalitis : a case report and literature review update. Neurol Sci. 2024;45(1):83-92. DOI: 10.1007/s10072-023-07034-x
19. Wurdack K, Prüss H, Finke C. Evolution from viral encephalitis to autoimmune encephalitis to multiple sclerosis: a case report. J Neurol. 2024;271:7035-7038. DOI: 10.1007/s00415-024-12659-9
20. Tao S, Zhang Y, Ye H, Guo D. AQP4-IgG-seropositive neuromyelitis optica spectrum disorder (NMOSD) coexisting with anti-N-methyl-D-aspartate receptor (NMDAR) encephalitis : A case report and literature review. Mult Scler Relat Disord. 2019;35:185-192. DOI: 10.1016/j.msard.2019.07.008
21. Yin XJ, Zhang LF, Bao LH, Feng ZC, Chen JH, Li BX, et al. Overlapping syndrome of recurrent anti-N-methyl-D-aspartate receptor encephalitis and anti-myelin oligodendrocyte glycoprotein demyelinating diseases: A case report. World J Clin Cases. 2022;10(18):6148-6155. DOI: 10.12998/wjcc.v10.i18.6148
Об авторах
Ю. Н. СорокинРоссия
Юрий Николаевич Сорокин, д. м. н., доцент; профессор
кафедра неврологии и восстановительной медицины с курсом остеопатии
Ростов-на-Дону
Е. Ю. Сорокина
Россия
Елена Юрьевна Сорокина, старший преподаватель
кафедра иностранных языков с курсом латинского языка
Ростов-на-Дону
Рецензия
Для цитирования:
Сорокин Ю.Н., Сорокина Е.Ю. Аутоиммунные энцефалиты: взгляд невролога (сложные вопросы диагностики). Южно-Российский журнал терапевтической практики. 2025;6(1):19-26. https://doi.org/10.21886/2712-8156-2025-6-1-19-26
For citation:
Sorokin Yu.N., Sorokina E.Yu. Autoimmune encephalitis: neurologist’s view (complex questions of diagnostics). South Russian Journal of Therapeutic Practice. 2025;6(1):19-26. (In Russ.) https://doi.org/10.21886/2712-8156-2025-6-1-19-26


























