Перейти к:
Трудности диагностики перипартальной кардиомиопатии на фоне новой коронавирусной инфекции при осложненном течении беременности: клинический случай
https://doi.org/10.21886/2712-8156-2025-6-3-103-111
Аннотация
Перипартальная кардиомиопатия, или кардиомиопатия Мидоуса, является нечастым, достаточно трудно диагностируемым заболеванием, развивающимся на последнем месяце беременности или в течение пяти месяцев послеродового периода. Ошибки в диагностике могут привести к постановке неправильного диагноза и, следовательно, к назначению неадекватного лечения, что чревато серьёзными последствиями. Наличие новой коронавирусной инфекции может приводить к изменению клинической картины и представлять определённые сложности для верификации диагноза. Данный клинический случай демонстрирует острое развитие сердечной недостаточности на фоне перипартальной кардиомиопатии у пациентки с новой коронавирусной инфекцией. При госпитализации на фоне характерных жалоб (одышка, чувство нехватки воздуха, отёки на ногах и выраженная слабость) было успешно проведен кесарево сечение. Дальнейшее обследование позволило установить диагноз «Перипартальная кардиомиопатия». Так как рассматриваемая патология является диагнозом исключения, необходимо проводить дифференциальную диагностику с такими заболеваниями, как латентно протекаюшая до беременности идиопатическая и семейная дилатационная кардиомиопатии, бессимптомные пороки сердца, тромбоэмболия лёгочной артерии. В лечении перипартальной кардиомиопатии особое внимание уделяется назначению бромокриптина как основы патогенетической терапии. Представленный клинический случай демонстрирует важность своевременности и правильности проведения диагностического поиска у пациенток с характерными жалобами на последнем месяце беременности или в послеродовом периоде, осложнённых присоединением новой коронавирусной инфекции.
Ключевые слова
Для цитирования:
Породенко Н.В., Заболотских Т.Б., Скибицкий В.В., Рязанцева Д.А., Ан К.Д., Крбащян А.А., Шрамко Я.Д. Трудности диагностики перипартальной кардиомиопатии на фоне новой коронавирусной инфекции при осложненном течении беременности: клинический случай. Южно-Российский журнал терапевтической практики. 2025;6(3):103-111. https://doi.org/10.21886/2712-8156-2025-6-3-103-111
For citation:
Porodenko N.V., Zabolotskikh T.B., Skibitskiy V.V., Ryazantseva D.A., An K.D., Krbaschyan A.A., Shramko Y.D. Difficulties in diagnosing peripartum cardiomyopathy with a background of a new coronaviral infection during the high-risk pregnancy. South Russian Journal of Therapeutic Practice. 2025;6(3):103-111. (In Russ.) https://doi.org/10.21886/2712-8156-2025-6-3-103-111
Введение
Перипартальная кардиомиопатия (ПКМП, кардиомиопатия Мидоуса) — редкая форма кардиомиопатии, развивающаяся в течение последнего месяца беременности или первых пяти месяцев послеродового периода. Она проявляется в виде сердечной недостаточностьи вследствие развития идиопатической систолической дисфункции левого желудочка [1]. Согласно некоторым зарубежным исследованиям, распространённость ПКМП составляет соответственно 1:2500–1:4000 беременных в США, 1:1000 в ЮАР и 1:300 в Гаити [2]. Точных данных о частоте развития ПКМП в Европе не имеется, что обусловлено редкой встречаемостью данной патологии. Систематически обобщённые данные о регистрации ПКМП в России отсутствуют. Имеются лишь единичные описания или исследования, посвященные данной проблеме [3][4].
Этиология и патогенез заболевания недостаточно изучены. Согласно последним исследованиям, основная этиопатогенетическая роль отводится пролактину массой 16 kDa [5]. В норме передней долей гипофиза вырабатывается пролактин 23 kDa [5]. Под действием оксидативного стресса в кардиомиоцитах активируется катепсин Д, который расщепляет пролактин 23 kDa до пролактина 16 kDa [5][6]. Эта форма пролактина обладает кардиотоксическим, провоспалительным, проапоптозным и антиангиогенным свойствами, ухудшая метаболизм и сократимость кардиомиоцитов [5]. Оксидативный стресс может развиться вследствие недостаточной экспрессии STAT-3 (активатор транскрипции и передатчик сигнала), который активирует фермент — марганцевую супероксиддисмутазу (MnSOD), являющуюся акцептором свободных радикалов кислорода, что ведёт к развитию оксидативного стресса, что было подтверждено в экспериментах на мышах и наблюдается при ПКМП [5][6].
Предрасполагающими факторами ПКМП являются возраст матери (подростковый или старше 30 лет), многоплодная беременность, двое и более родов в анамнезе, преэклампсия или эклампсия в анамнезе, длительная токолитическая терапия, негроидная раса, наследственная предрасположенность механизмов на развитие ПКМП [5][7]. Как правило, ПКМП — диагноз исключения. Критериями диагноза являются развитие сердечной недостаточности в конце беременности или в течение пяти месяцев после родов, наличие систолической дисфункции ЛЖ (ФВ ЛЖ <45%) и отсутствие другой причины сердечной недостаточности [8]. Необходимо проводить тщательную дифференциальную диагностику с латентно протекавшими заболеваниями, манифестацию которых провоцирует беременность: идиопатическая дилатационная КМП, семейная дилатационная КМП, бессимптомные пороки сердца, тромбоэмболия лёгочной артерии и др. [2][9]. Отличительной особенностью ПМКП является её быстрое прогрессирование и возникновение чаще в послеродовом периоде, в то время как перечисленные выше заболевания развиваются преимущественно во 2–3-м триместрах [5]. Заподозрить ПКМП бывает затруднительно, так как многие типичные для сердечной недостаточности симптомы (снижение толерантности к физической нагрузке, одышка, утомляемость, отёки на ногах) встречаются и при нормально протекающей беременности.
Вместе с тем развитие ПКМП у пациенток, перенёсших COVID-19 или на фоне течения новой коронавирусной инфекции, способно существенно затруднять установление диагноза. Тем более, что сама коронавирусная инфекция может осложняться развитием миокардита, перикардита и сопровождаться нарушением сократительной способности миокарда, приводя к коллизиям.
Редкая встречаемость ПКМП, отсутствие больших клинических исследований, недостаточная научная база случаев ПКМП, в том числе и у пациенток с COVID-19, делает, на наш взгляд, приведённый клинический случай интересным для медицинского сообщества. Также хотелось бы заметить, что этот случай ПКМП был диагностирован в стационаре Краевой клинической больницы скорой медицинской помощи г. Краснодара (ГБУЗ ККБСМП) впервые.
Описание клинического случая
Пациентка Т., 18 лет, 36 недель беременности, поступила в отделение патологии беременных ГБУЗ ККБСМП 02.06.2021 г. с жалобами на одышку, чувство нехватки воздуха, отёки на ногах и выраженную слабость.
От пациентки получено письменное информированное добровольное согласие на публикацию описания клинического случая и фотоматериалов (дата подписания — 18 марта 2024 г.).
Анамнез заболевания. Со слов пациентки: жалобы на одышку при физической нагрузке, ходьбе, в покое, особенно в горизонтальном положении, утомляемость, отёки появились в течение последней недели, приступообразный кашель стал беспокоить в течение последних 3-х дней. Беременность первая. Жалоб в предшествующий период беременности и до беременности пациентка не предъявляла.
Анамнез жизни. Жила и росла в благоприятных условиях. Перенесённые детские инфекции, вирусные гепатиты, венерические заболевания, недавние острые вирусные эпизоды отрицает. Наличие хронических заболеваний отрицает. Туберкулёзом болела, но, со слов пациентки, вылечилась. Имеется заключение фтизиатра: клиническое излечение очагового туберкулеза С6 правого лёгкого с исходом в незначительные посттуберкулёзные изменения в виде единичного мелкого плотного очага в С6 правого лёгкого. Вредные привычки отрицает. Аллергологический и наследственный анамнез не отягощены.
Физикальные данные. Состояние средней степени тяжести. Кожные покровы бледные. Отёки голеней, стоп, бедер, предплечий, кистей. Перкуторно над лёгкими лёгочный звук, местами притупление в нижних отделах. Аускультативно дыхание жесткое. ЧДД — 24 в минуту. Сатурация — 94%. АД — 135/100 мм рт. ст. ЧСС — 105 в минуту. Тоны сердца звучные, ритм правильный. Отмечается пульсация вен шеи. Живот увеличен в размере за счёт беременности (двойня), в верхних отделах безболезненный при пальпации. Печень не пальпируется. Симптом поколачивания отрицателен с обеих сторон.
Предварительный диагноз. Беременность 36 недель. Умеренная преэклампсия. Хроническая фетоплацентарная недостаточность (субкомпенсированная). Прогрессирующая внутриутробная гипоксия плодов. Двойня. Многоводие. Анемия средней степени. Клиническое излечение очагового туберкулеза С6 правого лёгкого с исходом в незначительные посттуберкулёзные изменения в виде единичного мелкого плотного очага в С6 правого лёгкого.
Временная шкала. Хронология развития заболевания пациентки Т. представлена на рисунке 1.
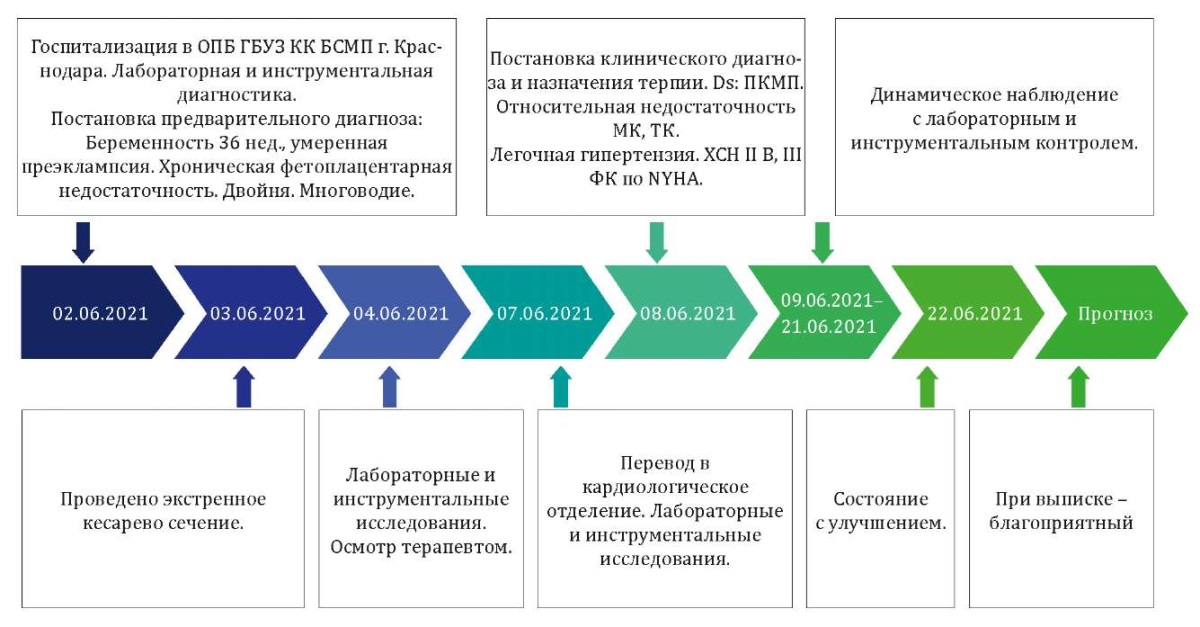
Рисунок 1. Хронология развития заболевания у пациентки Т.: ключевые события и прогноз
Figure 1. Patient T.: course of disease, key events and prognosis
Примечание: блок-схема временной шкалы выполнена авторами (согласно рекомендациям CARE). Сокращения: ОПБ — отделение патологии беременных; ГБУЗ ККБСМП — Государственное бюджетное учреждение здравоохранения «Краевая клиническая больница скорой медицинской помощи» Министерства здравоохранения Краснодарского края.
Note: the schematic diagram was performed by the authors (according to SCARE recommendations). Abbreviation: ОПБ (OPB) — department of pathology of pregnant women; ГБУЗ КК БСМП (GBUZ KK BSMP) — Regional Clinical Emergency Hospital, Krasnodar Krai.
Диагностические/лечебные процедуры. Анализ результатов общих анализов крови за период с 02.06.2021 по 04.06.2021 помог установить сниженние уровеней гемоглобина, эритроцитов, эритроцитарных индексов (MCV, MCH, MCHC), что свидетельствовало об анемии средней степени. Также наблюдался лейкоцитоз с нейтрофилезом и лимфопения. Биохимическом анализе выявлены гипопротеинемия за счёт снижения фракции альбуминов, гипербилирубинемия за счёт прямого билирубина, повышение печёночных ферментов, ЛДГ и СРБ. В коагулограмме был только повышен уровень фибриногена. В общем анализе мочи обнаружена незначительная протеинурия (до 0,3 г/л). Молекулярно-генетическое исследование (ПЦР) РНК 2019-nCoV (при поступлении от 02.06.2021 г.) — мазок отрицательный.
Медицинские вмешательства. Учитывая состояние пациентки 03.06.2021 г. медицинский консилиум принял решение о необходимости проведения экстренного родоразрешения и больной выполнено кесарево сечение по стандартной методике с лапаротомией по Пфанненштилю.
На первые (04.06.2021) и третьи (06.06.2021) сутки послеоперационного периода проведён осмотр терапевта. Состояние оценили как средней степени тяжести. Кожный покров бледный. Отёки голеней, стоп, бедер, предплечий, кистей. Перкуторно: над лёгкими легочный звук, местами притупление. Аускультативно: дыхание жёсткое, в межлопаточном пространстве крепитирующие рассеянные хрипы. ЧДД — 24 в минуту. Сатурация — менее 95% (до 92%). АД —135/90 мм рт.ст. ЧСС — 115 в минуту. Тоны сердца звучные, ритм правильный. Отмечается пульсация вен шеи; увеличение печени (выступает из-под края реберной дуги на 4–6 см по линиям), мягкоэластичной консистенции, болезненная при пальпации. Тяжесть состояния обусловлена сердечной недостаточностью, дыхательной недостаточностью, анемией средней степени на фоне умеренной преэклампсии нефротического синдрома.
Лабораторные данные за 07.06.2021 показали в анализе крови повышение гемоглобина до 95 г/л; в биохимии снижение общего билирубина, нормализация печёночных ферментов и СРБ. В коагулограмме фибриноген снизился с 9,77 до 6,04 г/л. В моче повысился уровень белка до 3,0 г/л. Анализ на Тропонин I (HS) показал увеличение до 6,8 нг/мл (реф. интервал — до 0,5 нг/мл). Серологическое исследование на антитела к SARS-CoV-2 положительный результат на Ig M.
На рисунках 2–7 представлены результаты компьютерной томографии лёгких от 04.06.2021 г.
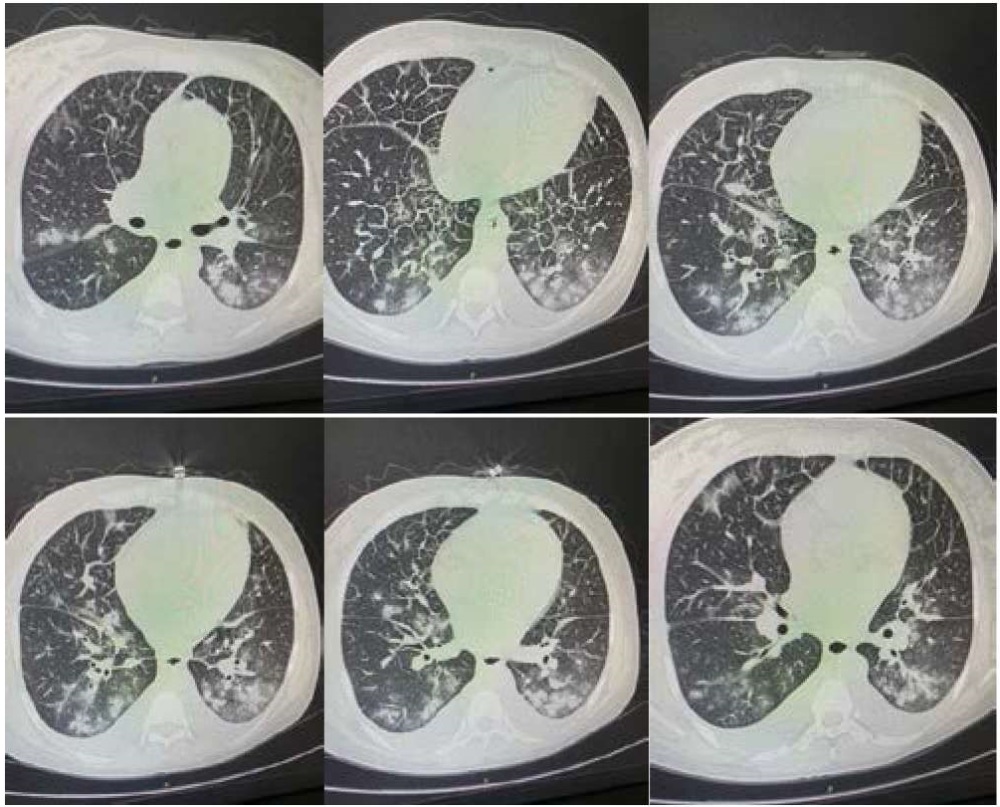
Рисунки 2–7. Результаты КТ лёгких пациентки Т. (04.06.2021)
Figure 2–7. The results of СТ scans of the lungs of a patient T. (04.06.2021)
На сканах лёгкие уменьшены в объёме за счёт наличия в обеих плевральных полостях жидкости толщиной слоя справа до 18 мм, слева до 20 мм. Полисегментарно в обоих лёгких определяются участки перибронхиальной инфильтрации. Диффузное утолщение междолькового интерстиция в обоих лёгких. В полости перикарда жидкость толщиной слоя до 9 мм. Заключение: двусторонняя полисегментарная пневмония. КТ-картина не исключает формирующегося отёка лёгких. Двусторонний гидроторакс, гидроперикард.
На ЭКГ от 07.06.2021 cинусовая тахикардия (130 в мин.).
Эхокардиография (07.06.2021). Левое предсердие (ЛП): 50 мм, конечный диастолический размер левого желудочка (КДР ЛД) — 55–56 мм. Фракция выброса (ФВ) ЛЖ — 36–38%. Локальная сократимость миокарда ЛЖ не нарушена. Правые отделы не расширены. Допплерография: митральная (++/+++) (МР) и трикуспидальная (++) (ТР) регургитация. Лёгочная артерия (ЛА): лёгочная гипертензия до 55–60 мм рт. ст. ЭХО-негативное пространство — следы жидкости (2–4 мм за задней створкой ЛЖ). Плевральные полости: с обеих сторон на уровне 7 межреберья жидкость толщиной слоя до 50–60 мм. Заключение: признаки дилатации ЛП, начальной дилатации ЛЖ, значительное снижение глобальной сократимости ЛЖ. Недостаточность МК, ТК, лёгочная гипертензия. Следы жидкости в полости перикарда, двусторонний гидроторакс. На рисунках 8–10 представлены данные эхокардиографии (ЭХОКГ) пациентки.
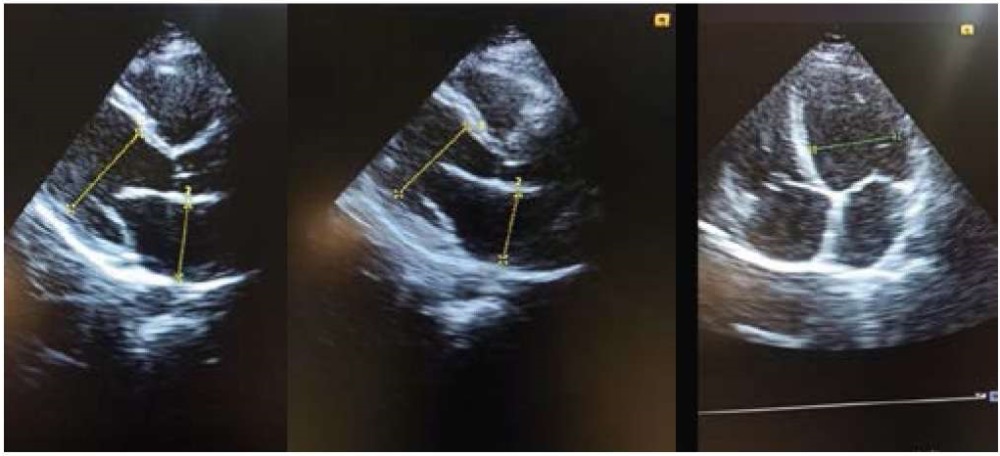
Рисунок 8–10. Данные эхокардиографии пациентки Т. (07.06.2021)
Figure 8–10. The results of ultrasound research (Echocardiography) of a patient T. (07.06.2021)
На рисунках 11–16 представлены результаты КТ грудной клетки (15.06.2021): наблюдается положительная динамика двусторонней полисегментарной пневмонии (вирусная, КТ 1). Малый гидроперикард.
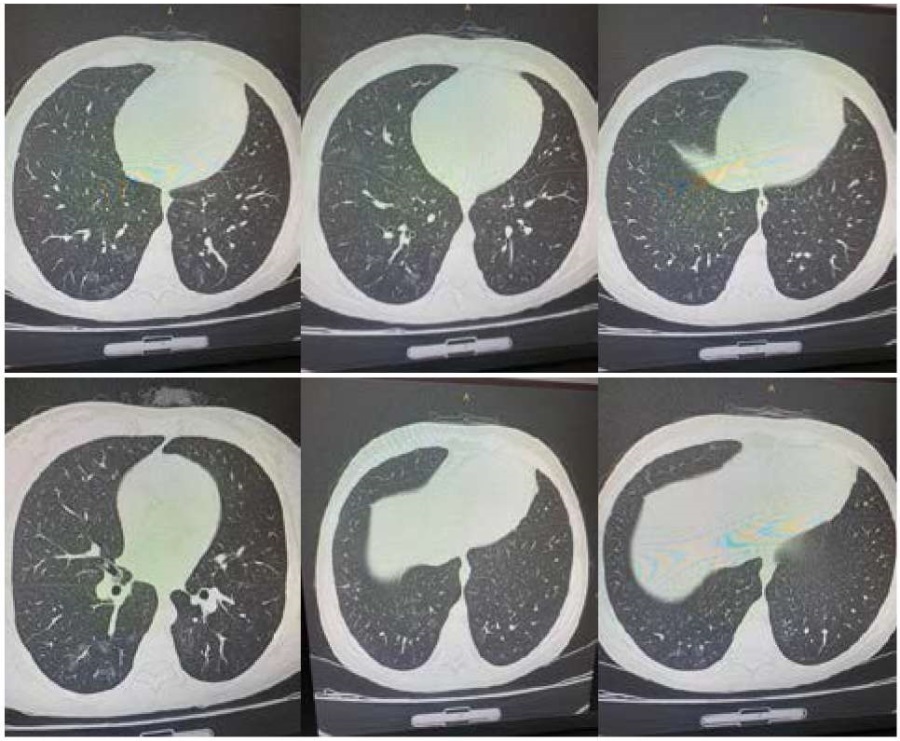
Рисунок 11–16. Результаты КТ лёгких пациентки Т. в динамике (15.06.2021)
Figure 11–16. CТ scans of the lungs of a patient T. in dynamics (15.06.2021)
УЗИ органов брюшной полости (от 16.06.2021): выявлены признаки гепатоспленомегалии. Диффузные изменения в паренхиме печени.
ЭХОКГ (21.06.2021): ЛП — 34 мм. КДР — 53 мм. ФВ — 45–47%. ТМЖП — 9–10 мм. ТЗСЛЖ — 9 мм. Зон нарушения локальной сократимости миокарда не выявлено. МР ++. ПЖ — не расширен, ПП — не расширено. ТР +/++. Клапан ЛА — без признаков ЛГ. Плевральные полости — свободной жидкости не определяется. Заключение: умеренное снижение общей сократимости миокарда ЛЖ. Умеренная недостаточность МК.
Клинический диагноз
После сопоставления жалоб, результатов физикального исследования, результатов лабораторно-инструментальных данных был установлен клинический диагноз.
Основной диагноз: Беременность 36 недель.
Фоновый: Новая коронавирусная инфекция, вирус ПЦР не идентифицирован (Ig M положительный).
Осложнения: Умеренная преэклампсия. Хроническая фетоплацентарная недостаточность (субкомпенсированная). Прогрессирующая внутриутробная гипоксия плодов. Двойня. Многоводие. Перипартальная кардиомиопатия с сердечной недостаточностью со сниженной фракцией выброса (ФВ 36–38% с исходом в ФВ 45–47%), III ФК. Относительная недостаточность митрального, трикуспидального клапанов. Лёгочная гипертензия. Двусторонняя полисегментарная пневмония, сочетанного генеза, тяжёлой степени. Гидроторакс. ДН II ст. Анемия гипохромная смешанного генеза, средней степени.
Оперативное вмешательство: лапаротомия по Пфанненштилю, кесарево сечение в нижнем сегменте (03.06.2021). Кровопотеря — 600 мл. Послеродовой период.
Медикаментозная терапия
Согласно поставленному диагнозу, пациентке было проведено лечение: Амоксициллин + клавулановая кислота 1200 мг 3 раза в сутки внутривенно, Левофлоксацин 500 мг 2 раза в сутки внутривенно, глюкозо-калиево-инсулиновая смесь 1 раз в сутки внутривенно капельно, Альбумин человеческий 10% 1 г/10 мл внутривенно капельно, Окситоцин 5 МЕ внутримышечно, Эноксапарин натрия 0,4 мл 2 раза в сутки подкожно. Перорально были назначены Бромокриптин 2,5 мг 1 раз в день, Спиронолактон 25 мг по 4 таблетки утром, Бисопролол 5 мг по 1 таблетке утром, Периндоприл 5 мг по 1 таблетке 1 раз в день, Торасемид 20 мг 1 раз в сутки, Дигоксин 0,25 мг 1 раз в день, Омепразол 20 мг 1 раз в день до еды, Гриппферон капли назальные по 3 капли в каждый носовой ход 5 раз в день.
Динамика и исходы
После родоразрешения и на фоне проводимой терапии у пациентки регрессировали отёки, исчезла одышка, уменьшилась общая слабость, недомогание, увеличилась переносимость физической нагрузки, нормализовались размеры печени, ЧСС. Сравнивая результаты ЭХОКГ, выявлена положительная динамика: увеличилась фракция выброса ЛЖ (с 3–38% до 45–47%), исчезли лёгочная гипертензия, дилатация полости ЛП и ЛЖ, снизилась регургитация на ТК. Побочных эффектов терапии не наблюдалось, лечение перенесла хорошо. Пациентка выписана в удовлетворительном состоянии, с отсутствием проявлений сердечной и дыхательной недостаточности, разрешением двусторонней пневмонии и регрессом нефропатии. Рекомендовано продолжить приём бисопролола 5 мг, периндоприла 5 мг, спиронолактона 25 мг, торасемида 10 мг с последующей отменой.
Через 6 и 12 месяцев выполнены ЭХОКГ и ЭКГ.
ЭХОКГ через 6 месяцев: ЛП — 31 мм. КДР — 46 мм. ФВ — 52%. ТМЖП — 9 мм. ТЗСЛЖ — 7 мм. Зон нарушения локальной сократимости нет. МР+. ПЖ не расширен, ПП не расширено. ТР+. Клапан ЛА без признаков ЛГ. Плевральные синусы свободны. Заключение: митральная регургитация, трикуспидальная регургитация.
ЭКГ: нормальное положение электрической оси, ритм синусовый, ЧСС — 84 в минуту.
ЭХОКГ через 12 месяцев: ЛП — 30 мм. КДР — 39 мм. ФВ — более 55%. ТМЖП — 8 мм. ТЗСЛЖ — 7 мм. В остальном без патологии. Заключение: гемодинамически значимые изменения не выявлены.
ЭКГ: нормальное положение электрической оси, ритм синусовый, ЧСС — 64 в минуту.
Прогноз
Прогноз для жизни и работы благоприятный при соблюдении всех назначенных рекомендаций. Прогноз относительно повторной беременности неоднозначный, требуется тщательное обследование и постоянный контроль со стороны акушера-гинеколога и кардиолога. В литературе отсутствуют абсолютные противопоказания к повторной беременности.
Обсуждение
В представленном клиническом случае развитие ПКМП произошло остро, на фоне нормально протекавшей беременности. Из факторов риска можно выделить беременность двойней, многоводие, умеренную преэклампсию, факт первой беременности и молодой возраст (18 лет). Следует отметить, что состояние пациентки осложнилось развившейся пневмонией на фоне новой коронавирусной инфекции, что могло повлиять на развитие ПКМП, а также значительно ухудшить её течение. Вместе с тем, учитывая, что звенья патогенеза SARS-CoV-2 до сих пор продолжают изучаться, сказать точно, какую роль сыграл коронавирус в развитии и прогрессировании ПКМП не представляется возможным.
Выполнение родоразрешения позволило применить для терапии сердечной недостаточности препараты, соответствующие клиническим рекомендациям с включением в схему бромокриптина, что сопровождалось регрессией симптомов и эхокардиографической динамикой с полной нормализацией параметров через 6 и 12 месяцев.
Как известно, одним из основным звеньев патогенеза ПКМП является нарушение обмена пролактина. Включение в терапию бромокриптина, являющегося агонистом дофамина D2 рецепторов, ингибирует выработку пролактина, подавляя лактацию [5][10]. Согласно результатам проведённых исследований, бромокриптин улучшает прогноз, замедляет прогрессирование заболевания и улучшает систолическую функцию миокарда [5][11]. Это было подтверждено и в нашем клиническом примере, где на фоне терапии с добавлением бромокриптина у пациентки увеличилась сократимость с 36% до 47%, и в динамике через 6 и 12 месяцев наблюдалась полная нормализация ФВ. С учётом высокого риска тромбоэмболических осложнений на фоне терапии бромокриптином необходимо назначение антикоагулянтов [5][12][13]. В данном клиническом случае был использован эноксапарин натрия в дозировке 0,4 мл 2 раза в сутки подкожно.
Родоразрешение при ПКМП можно проводить и через естественные пути, но у пациентки по решению консилиума было выполнено кесарево сечение по акушерским показаниям [14].
В целом к моменту выписки состояние женщины было стабильным, регрессировали явления пневмонии, улучшились лабораторные данные, результаты ЭХОКГ, что свидетельствовало о правильно проведенном диагностическом поиске и назначенной терапии.
Учитывая, что снижение глобальной сократимости может наблюдаться в течение 5 и более месяцев, контрольные исследования были выполнены в нашем случае через 6 и 12 месяцев. Уже через полгода систолическая функция ЛЖ вернулась к норме.
Хотим ещё раз отметить, что ПКМП была и остаётся редким состоянием и диагнозом исключения, причины и факторы риска которого не до конца установлены. Вклад коронавирусной инфекции в развитие ПКМП остается также малоизученным. Вместе с тем ряд исследователей отмечает повышение заболеваемости ПКМП среди пациенток, перенёсших СOVID-19 [15]. Авторы отмечают, что наличие бессимптомного или малосимптомного течения коронавирусной инфекции во время беременности может способствовать вовлечению в патологический процесс сердца. Это может быть связано с повреждением эндотелия, развитием миокардита или иных нарушений. Нельзя исключить и факт генетических нарушений, приводящих к ПКМП. Перенесённая коронавирусная инфекция, даже с изначально лёгким течением COVID-19, может предрасполагать беременных к развитию ПКМП и должно рассматриваться как фактор риска при оценке пациенток с новыми симптомами сердечной недостаточности. Безусловно, необходимы дальнейшие исследования для подтверждения этой гипотезы и полного определения основной патофизиологии.
Дисфункция левого желудочка у пациенток с ПКМП может сохраняться не только первые 5 месяцев после родов, но и в более поздние сроки, что демонстрирует необходимость исследований в динамике. У лиц негроидной расы, по данным литературы, восстановление систолической дисфункции происходит в два раза дольше, и в два раза чаще они имеют постоянное снижение фракции выброса, чем лица европеоидной расы [16]. Эта генетическая предрасположенность может наблюдаться в 15% случаев, что диктует необходимость выполнять генетическое тестирование пациенток при планировании беременности.
Оптимизация лекарственной терапии ПКМП остаётся важной проблемой. Основными группами препаратов являются средства, применяемые у пациентов с сердечной недостаточностью с низкой или умеренно сниженной фракцией выброса. Однако беременность является фактором, ограничивающим использование ряда лекартсвенных препаратов. Так, возможно назначение бета-блокаторов, гидралазина, диуретиков, изосорбида динитрата. Но есть противопоказания для использования блокаторов ренин-ангиотензин-альдостероновой системы во время беременности. При грудном вскармливании большинство стандартных лекарств приемлемо, однако информация о безопасности пока недоступна для сакубитрил-вальсартана и ингибиторов натрий-глюкозного ко-транспортера 2 типа. Также необходимо проводить антикоагулянтную поддержку. Продолжается изучение использования бромокриптина у этой категории пациенток.
Последующие планирования беременностей женщин, перенёсших ПКМП, остаётся сложной задачей и должно проводиться коллегиально, специальной командой специалистов.
Заключение
Ведение пациенток с ПКМП должно включать в себя тщательную диагностику и дифференциальную диагностику, в ряде случаев — генетическое тестирование, выбор оптимальной лекарственной терапии, особенно учитывая гравидарный статус. Следует помнить, что беременность может легко маскировать симптомы развивающегося заболевания. Влияние коронавирусной инфекции на развитие и течение ПКМП является непредсказуемым. Представленный клинический случай, на наш взгляд, может оказаться полезным для специалистов разных профилей. Требуются дальнейшие исследования в рамках данного вопроса.
Список литературы
1. Johnson-Coyle L, Jensen L, Sobey A; American College of Cardiology Foundation; American Heart Association. Peripartum cardiomyopathy : review and practice guidelines. Am J Crit Care. 2012;21(2):89-98. Erratum in: Am J Crit Care. 2012;21(3):155. Dosage error in article text. PMID: 22381985. DOI: 10.4037/ajcc2012163.
2. Sliwa K, Hilfiker-Kleiner D, Petrie MC, Mebazaa A, Pieske B, Buchmann E, et al. Current state of knowledge on aetiology, diagnosis, management, and therapy of peripartum cardiomyopathy: a position statement from the Heart Failure Association of the European Society of Cardiology Working Group on peripartum cardiomyopathy. Eur J Heart Fail. 2010;12(8):767-778. DOI: 10.1093/eurjhf/hfq120
3. Голицына Н.А., Ильина Т.Е., Королева Л.Ю., Аминева Н.В., Боровков Н.Н. Клиническое наблюдение перипартальной кардиомиопатии. Клин. мед. 2016;94(11):865—868. DOI: 10.18821/0023-2149-2016-94-11-865-868
4. Корнеева Н.В., Мислимова Н.Н. Клинический случай успешного лечения перипартальной кардиомиопатии. Кардиоваскулярная терапия и профилактика. 2024;23(7):4080. DOI: 10.15829/1728-8800-2024-4080
5. Honigberg MC, Givertz MM. Peripartum cardiomyopathy. BMJ. 2019;364:k5287. DOI: 10.1136/bmj.k5287
6. Hilfiker-Kleiner D, Kaminski K, Podewski E, Bonda T, Schaefer A, Sliwa K,et al. A cathepsin D-cleaved 16 kDa form of prolactin mediates postpartum cardiomyopathy. Cell. 2007;128(3):589-600. DOI: 10.1016/j.cell.2006.12.036
7. Hilfiker-Kleiner D, Sliwa K. Pathophysiology and epidemiology of peripartum cardiomyopathy. Nat Rev Cardiol. 2014;11(6):364-370. DOI: 10.1038/nrcardio.2014.37
8. Davis MB, Arany Z, McNamara DM, Goland S, Elkayam U. Peripartum Cardiomyopathy : JACC State-of-the-Art Review. J Am Coll Cardiol. 2020;75(2):207-221. DOI: 10.1016/j.jacc.2019.11.014
9. Pearson GD, Veille JC, Rahimtoola S, Hsia J, Oakley CM, Hosenpud JD, et al. Peripartum cardiomyopathy : National Heart, Lung, and Blood Institute and Office of Rare Diseases (National Institutes of Health) workshop recommendations and review. JAMA. 2000;283(9):1183-1188. DOI: 10.1001/jama.283.9.1183
10. Arbelo E, Protonotarios A, Gimeno JR, Arbustini E, Barriales-Villa R, Basso C, et al. 2023 ESC Guidelines for the management of cardiomyopathies. Eur Heart J. 2023;44(37):3503-3626. DOI: 10.1093/eurheartj/ehad194
11. Elkayam U, Goland S. Bromocriptine for the treatment of peripartum cardiomyopathy. Circulation. 2010;121(13):1463-1464. DOI: 10.1161/CIR.0b013e3181db2f07
12. Haghikia A, Podewski E, Libhaber E, Labidi S, Fischer D, Roentgen P, et al. Phenotyping and outcome on contemporary management in a German cohort of patients with peripartum cardiomyopathy. Basic Res Cardiol. 2013;108(4):366. DOI: 10.1007/s00395-013-0366-9
13. Hilfiker-Kleiner D, Haghikia A, Berliner D, Vogel-Claussen J, Schwab J, Franke A, et al. Bromocriptine for the treatment of peripartum cardiomyopathy: a multicentre randomized study. Eur Heart J. 2017;38(35):2671-2679. DOI: 10.1093/eurheartj/ehx355
14. Maurel C, Abhay K, Schaeffer A, Lange F, Castot A, Melon E. Acute thrombotic accident in the postpartum period in a patient receiving bromocriptine. Crit Care Med. 1990;18(10):1180-1181. DOI: 10.1097/00003246-199010000-00026
15. Фалевко С.Ю., Бигашев А.Р., Цечоева Л.Ш., Дудова К.А. Клинический случай успешного ведения пациентки с перипартальной кардиомиопатией на 38-ой неделе беременности. Журнал «Неотложная хирургия» им. И.И. Джанелидзе. 2025;(1):130–136.
16. Yaniv-Salem S, Dym L, Nesher L, Zahger D, Shalev A, Shmueli H. Post-COVID-19 Peripartum Cardiomyopathy: Experience from a Large Tertiary Referral Center. Isr Med Assoc J. 2023;25(8):533-537. PMID: 37574890.
17. Arany Z. Peripartum Cardiomyopathy. N Engl J Med. 2024;390(2):154-164. DOI: 10.1056/NEJMra2306667
Об авторах
Н. В. ПороденкоРоссия
Наталья Валерьевна Породенко, к. м. н., доцент, доцент кафедры
кафедра госпитальной терапии
Краснодар
Т. Б. Заболотских
Россия
Татьяна Борисовна Заболотских, к. м. н., доцент
кафедра госпитальной терапии
Краснодар
В. В. Скибицкий
Россия
Виталий Викентьевич Скибицкий, д. м. н., профессор, профессор кафедры
кафедра госпитальной терапии
Краснодар
Д. А. Рязанцева
Россия
Диана Алексеевна Рязанцева, клинический ординатор
ФПК и ППС; кафедра Терапии № 1
Краснодар
К. Д. Ан
Россия
Константин Дмитриевич Ан, клинический ординатор
ФПК и ППС; кафедра Хирургии № 2
Краснодар
А. А. Крбащян
Россия
Ангелина Альбертовна Крбащян, клинический ординатор
ФПК и ППС; кафедра Лучевой Диагностики № 1
Краснодар
Я. Д. Шрамко
Россия
Яна Дмитриевна Шрамко, студентка 6 курса
Краснодар
Дополнительные файлы
Рецензия
Для цитирования:
Породенко Н.В., Заболотских Т.Б., Скибицкий В.В., Рязанцева Д.А., Ан К.Д., Крбащян А.А., Шрамко Я.Д. Трудности диагностики перипартальной кардиомиопатии на фоне новой коронавирусной инфекции при осложненном течении беременности: клинический случай. Южно-Российский журнал терапевтической практики. 2025;6(3):103-111. https://doi.org/10.21886/2712-8156-2025-6-3-103-111
For citation:
Porodenko N.V., Zabolotskikh T.B., Skibitskiy V.V., Ryazantseva D.A., An K.D., Krbaschyan A.A., Shramko Y.D. Difficulties in diagnosing peripartum cardiomyopathy with a background of a new coronaviral infection during the high-risk pregnancy. South Russian Journal of Therapeutic Practice. 2025;6(3):103-111. (In Russ.) https://doi.org/10.21886/2712-8156-2025-6-3-103-111


























