Перейти к:
Клинический случай аритмогенной дисплазии правого желудочка
https://doi.org/10.21886/2712-8156-2021-2-1-109-114
Аннотация
Аритмогенная дисплазия правого желудочка (АДПЖ) относится к наследственным заболеваниям миокарда, при котором отмечаются структурные и функциональные нарушения в миокарде правого желудочка, вызывающие нарушения ритма и проводимости, в том числе фатальные желудочковые аритмии. АДПЖ считается одной из наиболее частых причин внезапной сердечной смерти у молодых людей и лиц, занимающихся спортом. Однако в практике встречаются случаи данного заболевания и у лиц более старшей возрастной категории. Диагностика АДПЖ по-прежнему вызывает трудности в связи с возможным длительным бессимптомным течением заболевания. В статье описан клинический случай АДПЖ у мужчины 48 лет.
Для цитирования:
Соловьева Е.В., Попова Н.А., Власова Т.В., Горбунова М.Л., Анцыгина Л.Н. Клинический случай аритмогенной дисплазии правого желудочка. Южно-Российский журнал терапевтической практики. 2021;2(1):109-114. https://doi.org/10.21886/2712-8156-2021-2-1-109-114
For citation:
Solovyoval E.V., Popova N.A., Vlasoval T.V., Gorbunova M.L., Antsygina L.N. A clinical case of arrhythmogenic right ventricular dysplasia. South Russian Journal of Therapeutic Practice. 2021;2(1):109-114. (In Russ.) https://doi.org/10.21886/2712-8156-2021-2-1-109-114
Аритмогенная дисплазия правого желудочка (АДПЖ), или аритмогенная кардиомиопатия правого желудочка, — прогрессирующее наследственное заболевание сердечной мышцы. Характеризуется очаговым фиброзно-жировым перерождением миокарда правого желудочка в пределах так называемого треугольника дисплазии, находящегося между выносящим, приносящим путём правого желудочка и верхушкой сердца, клинически проявляется желудочковыми нарушениями ритма, в том числе пароксизмальной желудочковой тахикардией (ЖТХ) [1, 2]. Однако в настоящее время жировая инфильтрация миокарда ПЖ не является патогномоничным признаком, поскольку она может встречаться у пожилых людей без заболевания. На фоне атрофии мышечной ткани продолжается разрушение кардиомиоцитов: наличие остаточных клеток — менее 60% (большой критерий), с фиброзным или жировым замещением или без него [3]. АДПЖ относится к редко встречающимся болезням, однако сопровождается высоким риском внезапной сердечной смерти (ВСС). В целом ряде исследований показана высокая инфицированность больных кардиотропными вирусами, такими как энтеровирус, парвовирус [3, 4].
Впервые клинику описал итальянский врачанатом Джованни-Мария Ланчизи. АДПЖ была описана как наследственное заболевание, наблюдающееся в четырех поколениях у всех членов одной семьи. Несмотря на то, что заболевание считается наследственным, генетическая причина развития патологии встречается менее чем в половине случаев [4].
У 60% пациентов с АДПЖ причиной заболевания являются мутации в генах, кодирующих десмосомные белки. В настоящее время известно более 100 генов и мутаций, принимающих участие в различных формах заболеваний сердца (гипертрофическая, дилатационная и аритмогенная кардиомиопатия) [4, 5]. В результате многочисленных исследований показано, что более 10% носителей мутаций генов десмосомных белков имеют высокий риск развития сложных аритмий и ВСС [6, 7].
Клинически АДПЖ характеризуется желудочковой тахикардией, блокадой проводящей системы сердца, дилатацией правого желудочка и сердечной недостаточностью.
В дебюте заболевание длительно может протекать бессимптомно, однако и в отсутствие специфической симптоматики высок риск жизнеугрожаемых аритмий.
При прогрессировании АДПЖ на первый план выходит ряд симптомов: перебои в работе сердца (>50% случаев), кардиалгии (46% случаев), сердцебиения (60% случаев), синкопальные состояния (40% случаев), ВСС (26% случаев) [8,9]. В клинике заболевания могут присутствовать такие признаки, как повышенная утомляемость, головокружение, одышка, снижение толерантности к физическим нагрузкам, указывающие на присутствие или прогрессирование сердечной недостаточности (СН).
Развитие АДПЖ имеет несколько стадий (латентную, электрических нарушений, правожелудочковой СН, бивентрикулярной СН).
Во время латентной стадии ВСC может быть первым и единственным проявлением, возникновение которой может провоцироваться активной физической нагрузкой. При развитии стадии электрических нарушений регистрируются нарушения ритма сердца и морфологические изменения правого желудочка. При прогрессировании процесса развивается диффузное поражение миокарда, которое может приводить к развитию бивентрикулярной сердечной недостаточности (СН), осложненной различными нарушениями ритма сердца (включая фибрилляцию предсердий). Финальная стадия процесса, как правило, представлена клиникой дилатационной кардиомиопатии [10].
В молодом возрасте АДПЖ является второй по частоте причиной внезапной смерти после ишемической болезни сердца [8].
Учитывая бессимптомное течение болезни или развитие ВСС как первого проявления, эпидемиологические данные остаются спорными. В среднем, заболевание встречается с частотой 6 на 10 тыс. жителей. По другим данным, АДПЖ является одной из самых распространенных кардиомиопатий и встречается, как минимум, у 200 пациентов в городе с населением 1 млн человек [8]. Отмечается, что болезнь чаще диагностируется у мужчин (около 80%) среднего возраста (до 40 лет) [5]. Считается, что у пациентов, страдающих АДПЖ, встречается примерно 17% случаев ВСС. Пристальное внимание стали уделять ранней диагностике заболевания у лиц, занимающихся спортом профессионально, после изучения причин ВВС у 16 молодых спортсменов E. Larsson и соавт. в 1999 г. В результате проведенного исследования выяснилось, что АДПЖ была обнаружена у каждого 4-го пациента. Однако возможно, что в данном случае частота встречаемости заболевания обусловлена более тщательным обследованием лиц данной категории. Начало тахикардии может быть отсрочено на многие годы, пока ПЖ значительно не увеличен, а размер аритмогенного субстрата недостаточно велик, чтобы вызвать постоянную желудочковую тахиаритмию.
Учитывая возможность длительного латентного течения АДПЖ, процесс диагностики остаётся сложным. Кроме стандартных методов обследования у пациентов с подозрением на АДПЖ в некоторых ситуациях показано проведение магниторезонансной томографии (МРТ), контрастной вентрикулографии сердца и эндомиокардиальной биопсии (ЭМБ). Для оценки структуры миокарда, а также электрических и функциональных изменений ПЖ проводится 3D-анатомическое картирование [10].
Прогноз заболевания напрямую зависит от своевременной профилактики внезапной сердечной смерти.
Представляем собственное наблюдение.
Пациент В., 48 лет, служащий, поступил в кардиологическое отделение Дорожной больницы на станции Нижний Новгород с жалобами на приступы сердцебиения, которые сопровождаются резкой слабостью, головокружением, чувством нехватки воздуха. С 45 лет отмечает перебои в работе сердца, за медицинской помощью не обращался. Ухудшение в течение трёх месяцев, когда появились вышеописанные приступы сердцебиения. Накануне госпитализации во время быстрой ходьбы возник подобный приступ, впервые была кратковременная потеря сознания.
В анамнезе редкие острые респираторные заболевания. Служил в армии. Физическая активность — умеренная, спортом не занимался. Не курит, алкоголь употребляет умеренно. Отец умер внезапно в 47 лет, причина неизвестна.
Результаты осмотра. Правильного телосложения, избыточного питания (индекс массы тела — 29,6 кг/м2). Кожные покровы чистые, обычной окраски. При аускультации легких дыхание везикулярное, хрипов нет. Частота дыхания — 16 в минуту. Тоны сердца ритмичные, приглушены, частота сердечных сокращений 78 уд/мин. Артериальное давление — 115/85 мм рт.ст. Печень не увеличена, периферических отёков нет.
По данным проведенных лабораторных исследований, клинические и биохимические анализы без патологии, NT-proВNP – 125 пг/мл (верхняя граница нормы).
Данные инструментальных методов обследования. ЭКГ: ритм синусовый, регулярный. ЧСС 76 уд/мин. Горизонтальное положение ЭОС. Нарушение внутрижелудочковой проводимости. Инверсия зубца Т в V1-V5. Эпсилон волна в V1-V3 (рис.1).
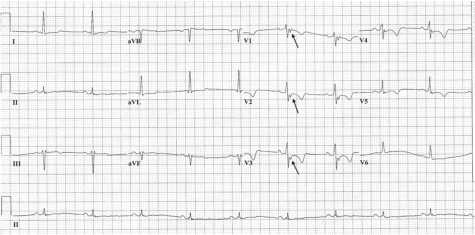
Рисунок 1. Электрокардиограмма больного В.: нарушение внутрижелудочковой проводимости, инверсия зубца Т V1-V5, эпсилон-волна V1-V3.
Холтеровское ЭКГ мониторирование: исследование проводилось в течение 22 часов. За сутки зафиксирован синусовый ритм. Средняя ЧСС 77 уд/мин, ЧСС минимальная (37 уд/мин.) — во время сна, ЧСС максимальная (168 уд/мин) — при ходьбе по лестнице. Желудочковая эктопическая активность представлена 3412 мономорфной желудочковой экстрасистолией (ЖЭС) с морфологией блокады левой ножки пучка Гиса (БЛНПГ), преимущественно в дневное время. Одиночных — 3308, по типу бигеминии — 54, парных — 37 ЖЭС. Зарегистрированы два эпизода неустойчивой желудочковой тахикардии (ЖТ) по 7 и 6 комплексов (рис. 2.). Пауз, изменений ST-T, интервала QT не выявлено.
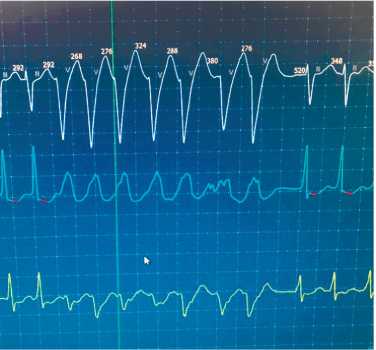
Рисунок 2. Холтеровское мониторирование больного В.: пароксизм неустойчивой ЖТ с частотой 214 уд/мин.
Рентгенография органов грудной клетки: воспалительных и очаговых изменений не выявлено. Плевральные синусы свободны. Легочный рисунок несколько усилен. Корни легких не изменены. Сердце расположено нормально, размеры не увеличены. Сосудистый пучок не изменен. Аорта без особенностей. Верхняя полая вена не расширена. Диафрагма без особенностей.
По данным трансторакальной эхокардиографии (ЭХО-КГ, рис. 3), выявлено расширение полости правого желудочка (ПЖ) со снижением его сократительной способности (фракция выброса ПЖ составила 39%), увеличение полости правого предсердия до 6,1 × 4,6 см и левого предсердия до 5,6 × 5,0 см. КДО ПЖ — 164 мл; КСО ПЖ — 102 мл. При изучении левого желудочка (ЛЖ) патологии выявлено не было, ФВ ЛЖ – 51%. Нижняя полая вена не расширена, диаметр — 2,0 см, коллабировала на вдохе более 50%. Данных о врождённом пороке сердца не выявлено.
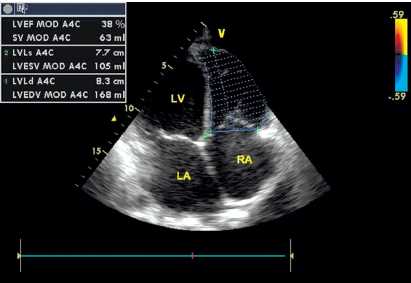
Рисунок 3. Эхокардиограмма больного В. Расширение предсердий и правого желудочка.
Примечание: ЛП — левое предсердие; ПП — правое предсердие; ЛЖ — левый желудочек; ПЖ — правый желудочек; КСР — конечно-систолический размер; КДР — конечно-диастолический размер; КСО — конечно-систолический объем; КДО — конечно-диастолический объем; ФВ — фракция выброса.
Диагностическая коронарография: данных о гемодинамически значимых стенозах коронарных артерий не получено.
Для уточнения состояния правых отделов сердца и исключения врождённых пороков была проведена магнитно-резонансная томография (МРТ) сердца с контрастным усилением гадолинием.
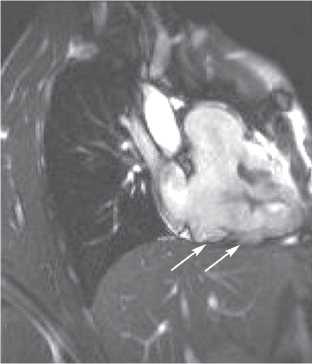
Рисунок 4. Магнитно-резонансная томограмма больного В. Дискинез передней стенки правого желудочка, микроаневризмы передней стенки правого желудочка, фаза диастолы.
Магнитно-резонансная томография с контрастным усилением. Сердце расположено типично. ПП 60× 45 мм (увеличено), левое предсердие 48 × 50 мм (увеличено). Увеличение правого желудочка: КДО — 166 мл, нормализованный показатель КДО (КДО/ площади поверхности тела (ППТ)) — 111 мл/м2, КСО ПЖ — 104 мл. Фракция выброса ПЖ — 39%. Отмечается гипокинез стенок ПЖ с мелкими участками истончения и дискинеза до 3–4 мм (микроаневризмы). Жировая инфильтрация миокарда ПЖ. ЛЖ: КДР ЛЖ — 45 мм, КСР ЛЖ — 34 мм, КДО ЛЖ — 155 мл, КСО ЛЖ — 68 мл, ФВ — 52%. Клапаны не изменены. Заключение: дилатация полостей правых отделов сердца, снижение сократительной способности ПЖ (ФВ — 39%); гипокинез с участками неравномерного истончения стенок ПЖ; жировая инфильтрация миокарда ПЖ.
При выполнении программируемой стимуляции правого желудочка был индуцирован пароксизм мономорфной желудочковой тахикардии (ЖТ), морфология которого была идентична «пробежкам» ЖТ, зарегистрированным при холтеровском мониторировании ЭКГ. Пароксизм самостоятельно купировался через 4 сек.
На основании клинической картины, результатов лабораторных и инструментальных методов исследования поставлен диагноз: Аритмогенная дисплазия правого желудочка. Синкопальное состояние от 13.04.2020 г.
Обсуждение
Приведённое наблюдение не является строго типичным для АДПЖ, поскольку большинство пациентов начинает предъявлять соответствующие жалобы (сердцебиение, головокружение, обморочные состояния) чаще в период между вторым и четвёртым десятилетием жизни (заболевание редко манифестирует до 10 лет). Однако наиболее типичным было появление симптомов на четвёртом десятилетии жизни. В нашем случае первые признаки заболевания (ощущение перебоев в работе сердца) проявились только в 45 лет. Синкопальное состояние впервые возникло во время интенсивной физической нагрузки (быстрая ходьба в гору). Четких указаний на семейный анамнез ВСС в молодом возрасте нет. При обследовании 18-летнего сына пациента (ЭКГ, включая холтеровское мониторирование, ЭхоКГ) патологии выявлено не было. Однако известно, что результаты ЭКГ могут быть нормальными в латентной фазе АДПЖ и проявляются при прогрессировании заболевания, а ЭКГ-признаки, типичные для АДПЖ, включая наличие эпсилон-волны (малоамплитудные сигналы между концом комплекса QRS и началом зубца Т) в отведениях V1 V3 (видны у 33%), могут носить преходящий характер. В начальной (скрытой) фазе структурные изменения могут отсутствовать или быть минимальными, однако риск ВСС уже повышен. Возможно более позднее проявление структурных изменений сердца, в том числе при присоединении воспалительных механизмов (миокардита). Хорошо известно «здоровое носительство» генных мутаций без клинических признаков АДПЖ или с мягкими их проявлениями, поэтому необходимо тщательное динамическое наблюдение за сыном пациента в течение жизни.
У 48-летнего пациента на ЭКГ обнаружены изменения в грудных отведениях в виде отрицательных зубцов Т в V1–V5, в большей степени в правых отведениях V1–V3 при отсутствии каких-либо указаний на наличие в анамнезе заболеваний сердца (в том числе каких-либо пороков сердца) и бронхо-легочной патологии, подозрение на эпсилон-волну в V1–V3. При холтеровском мониторировании ЭКГ обращено внимание на большое количество желудочковых экстрасистол, исходящих из правого желудочка. Трансторакальная ЭхоКГ выявила значительное увеличение правых камер сердца при интактности левого желудочка. Данных о пороках развития сердца и сосудов получено не было. С помощью МРТ сердца (при которой правый желудочек лучше визуализируется, чем на эхокардиографии) с контрастным усилением гадолинием подтверждено значительное увеличение правых камер сердца (КДО правого желудочка – 166 мл), уточнены их размеры, выявлено снижение фракции выброса правого желудочка (39%), что является одним из основных признаков АДПЖ. Такие изменения, как гипокинез с участками неравномерного истончения (микроаневризмы) стенок ПЖ, жировая инфильтрация миокарда ПЖ весьма специфичны для этого заболевания, как и локальный характер поражения, что наблюдалось у нашего пациента.
В настоящем случае отсутствует поражение левого желудочка. По данным литературы, бивентрикулярное поражение отмечается в 16% случаев и прогноз у этих пациентов хуже [9]. Для постановки диагноза АДПЖ, безусловно, наиболее важными были данные, полученные при МРТ сердца.
Для более точной диагностики заболевания в 2010 г. рабочей группой по заболеваниям миокарда и перикарда Европейского общества кардиологов были скорректированы диагностические критерии, которые включают в себя большие и малые критерии из следующих 6 различных категорий:
- региональная дисфункция и структурные изменения по данным Эхо-КГ, МРТ и/или ангиографии ПЖ;
- характеристика стенки по данным эндомиокардиальной биопсии;
- семейный анамнез (ВСС до 35 лет от АДПЖ);
- нарушения реполяризации по данным ЭКГ;
- нарушения деполяризации/проводимости по данным ЭКГ и/или сигналам усредненной ЭКГ аритмии по данным холтеровского мониторирования ЭКГ.
Точный диагноз определяется как присутствие 2 больших критериев, или 1 большого и 2 малых критериев, или 4 малых критериев.
Ниже приведены критерии, которые присутствуют у нашего пациента.
Большие критерии:
- региональный дискинез правого желудочка в сочетании со сниженной фракцией выброса (ФВПЖ - 39%);
- инвертированный Т-зубец в правых грудных отведениях V1–V3;
- эпсилон-волна в правых грудных отведениях V1–V3.
Малые критерии — желудочковые аритмии, ЖТХ с морфологией блокады ЛНПГ (ось сердца неопределенная) и/или ЖЭС ≥ 500/сут.
Таким образом, у пациента 3 больших критерия и 1 малый, что соответствует определенному диагнозу АДПЖ [11].
Жировая инфильтрация миокарда правого желудочка, определяемая у пациента, более не считается типичным признаком АДПЖ. Более специфичны нарушения кинетики правого желудочка. При эндомиокардиальной биопсии возможно выявление разрушающихся кардиомиоцитов с фиброзным и жировым замещением, атрофии мышечной ткани, но отсутствие этих изменений не отрицает возможность наличия АДПЖ, так как процесс носит очаговый характер. Эндомиокардиальная биопсия не является рутинным методом обследования из-за частичного повреждения миокарда, что приводит к низкой диагностической ценности.
Поскольку АДПЖ часто является причиной ВСС, её предупреждение чрезвычайно актуально у этих пациентов. К предикторам ВСС относятся следующие:
- индуцированная во время электрофизиологического исследования ЖТХ;
- неустойчивая ЖТХ, зафиксированная во время неинвазивной оценки/мониторинга;
- значительная дилатация или обширное вовлечение ПЖ;
- предшествующая остановка сердца в анамнезе;
- необъяснимые обмороки;
- вовлечение левого желудочка;
- мужской пол;
- раннее начало заболевания (ранее 5 лет).
В нашем случае присутствуют такие предикторы ВСС, как индуцированная во время электрофизиологического исследования желудочковая тахикардия; неустойчивая желудочковая тахикардия, зафиксированная во время мониторинга ЭКГ; необъяснимые обмороки, мужской пол. Безусловно, внезапная потеря сознания у больного носила аритмогенный характер и была обусловлена пароксизмом гемодинамически значимой желудочковой тахикардии, что, согласно современным рекомендациям по ВСС, является показанием к имплантации кардиовертера-дефибриллятора [12], что и было произведено. Инвазивное электрофизиологическое исследование может рассматриваться с целью стратификации риска ВСС [12]. Эффективность интервенционного лечения желудочковых тахикардий у пациентов с АДПЖ — низкая из-за очагового и прогрессирующего характера поражения, что не улучшает прогноз. С целью вторичной профилактики ВСС больному был имплантирован автоматический кардиовертердефибриллятор Medtronic GEM III VR 7231 Сх. За 6 месяцев наблюдения не отмечалось его срабатывания. Для уменьшения симптомов, обусловленных аритмией, и их частоты был назначен бетаадреноблокатор метопролол-сукцинат 100 мг/ сут. При повторном ЭКГ-мониторировании отмечалось некоторое снижение ЖЭС с 3412 до 2792, но субъективная переносимость их улучшилась. «Пробежки» ЖТХ не регистрировались. Пациенту рекомендовано избегать активных физических нагрузок и воздержаться от участия в соревновательных видах спорта, поскольку это может спровоцировать фатальные желудочковые аритмии.
Заключение
Представленный случай демонстрирует возможность достаточно позднего дебюта АДПЖ. Для улучшения прогноза заболевания необходима своевременная диагностика с комплексным использованием современных методов и адекватное лечение, направленное, прежде всего, на профилактику внезапной смерти.
Список литературы
1. Лутохина Ю.А., Благова О.В., Недоступ А.В., Шестак А.Г., За-клязьминская Е.В. Клинические формы (классификация) аритмогенной дисплазии правого желудочка: особенности диагностики и лечения. Российский кардиологический журнал. 2018;2(154):19-31. DOI: 10.15829/1560-4071-2018-2-19-31
2. Бокерия О.Л., Ле Т.Г. Аритмогенная дисплазия правого желудочка. Анналы аритмологии. 2015;12(2):89-99. DOI: 10.15275/annaritmol.2015.2.4
3. Chelko SP, Asimaki A, Andersen P, Bedja D, Amat-Alarcon N, DeMazumder D, et al. Central role for GSK3P in the pathogenesis of arrhythmogenic cardiomyopathy. JCI Insight. 2016;1(5):e85923. DOI: 10.1172/jci.insight.85923.
4. Ortiz-Genga MF, Cuenca S, Dal Ferro M, Zorio E, Salgado-Aranda R, Climent V, et al. Truncating FLNC Mutations Are Associated With High-Risk Dilated and Arrhythmogenic Cardiomyopathies. J Am Coll Cardiol. 2016;68(22):2440-2451. DOI: 10.1016/j.jacc.2016.09.927
5. Дупляков Д.В., Югзова А.В., Тутуров А.О. Особенности ведения пациентов с аритмогенной кардиомиопатией правого желудочка. Кардиология: новости, мнения, обучение. 2018;6(4):24-35. DOI: 10.24411/2309-1908-2018-14004.
6. Bosman LP, Sammani A, James CA, Cadrin-Tourigny J, Calkins H, van Tintelen JP, et al. Predicting arrhythmic risk in arrhythmogenic right ventricular cardiomyopathy: A systematic review and meta-analysis. Heart Rhythm. 2018;15(7):1097-1107. DOI: 10.1016/j.hrthm.2018.01.031
7. Brignole M, Moya A, de Lange FJ, Deharo JC, Elliott PM, Fanciulli A, et al. 2018 ESC Guidelines for the diagnosis and management of syncope. Eur Heart J. 2018;39(21):1883-1948. DOI: 10.1093/eurheartj/ehy037.
8. Calkins H., Corrado D., Marcus F. Risk Stratification in Arrhythmogenic Right Ventricular Cardiomyopathy. Circulation. 2017;136(21):2068-2082 DOI: 10.1161/CIRCULATIONAHA.117.030792.
9. Gilotra NA, Bhonsale A, James CA, Te Riele ASJ, Murray B, Tichnell C, et al. Heart Failure Is Common and UnderRecognized in Patients With Arrhythmogenic Right Ventricular Cardiomyopathy/Dysplasia. Circ Heart Fail. 2017;10(9):e003819. DOI: 10.1161/CIRCHEARTFAILURE.116.003819.
10. Kimura Y, Noda T, Matsuyama TA, Otsuka Y, Kamakura T, Wada M, et al. Heart failure in patients with arrhythmogenic right ventricular cardiomyopathy: What are the risk factors? Int J Cardiol. 2017;241:288-294. DOI: 10.1016/j.ijcard.2017.04.061.
11. Focardi M., Cameli M., Carbone S.F., Massoni A., De Vito R., Lisi M. et al. Traditional and innovative echocardiographic parameters for the analysis of right ventricular performance incomparison with cardiac magnetic resonance. Eur. Heart J. Cardiovasc. Imaging. 2015;6 (1):47-52. DOI: 10.1093/ehjci/jeu156.
12. Silvia P.G., Blomstrom-Lundqvist C., Mazzanti+ A., Bloma N., Borggrefe M., Camm J., et al. Рекомендации ESC по лечению пациентов с желудочковыми нарушениями ритма и профилактике внезапной сердечной смерти 2015. Российский кардиологический журнал. 2016;(7):5-86. DOI: 10.15829/1560-4071-2016-7-5-86
Об авторах
Е. В. СоловьеваРоссия
Соловьева Елена Витальевна - кандидат медицинских наук, доцент, кафедра терапии и кардиологии.
Нижний Новгород
Н. А. Попова
Россия
Попова Наталия Алексеевна - кандидат медицинских наук, доцент, кафедра терапии и кардиологии.
Нижний Новгород
Т. В. Власова
Россия
Власова Татьяна Владимировна - кандидат медицинских наук, доцент, кафедра терапии и кардиологии.
Нижний Новгород
М. Л. Горбунова
Россия
Горбунова Марина Леонидовна - кандидат медицинских наук, доцент, врач кардиолог.
Нижний Новгород
Л. Н. Анцыгина
Россия
Анцыгина Людмила Николаевна - кандидат медицинских наук, врач кардиолог.
Нижний Новгород
Рецензия
Для цитирования:
Соловьева Е.В., Попова Н.А., Власова Т.В., Горбунова М.Л., Анцыгина Л.Н. Клинический случай аритмогенной дисплазии правого желудочка. Южно-Российский журнал терапевтической практики. 2021;2(1):109-114. https://doi.org/10.21886/2712-8156-2021-2-1-109-114
For citation:
Solovyoval E.V., Popova N.A., Vlasoval T.V., Gorbunova M.L., Antsygina L.N. A clinical case of arrhythmogenic right ventricular dysplasia. South Russian Journal of Therapeutic Practice. 2021;2(1):109-114. (In Russ.) https://doi.org/10.21886/2712-8156-2021-2-1-109-114
JATS XML

























