ОБРАЩЕНИЕ К ЧИТАТЕЛЯМ
ОБЗОРЫ
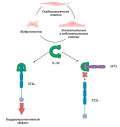
За последние десятилетия было разработано множество прогностических инструментов, однако идентификация биомаркеров, которые могут предсказать риск острой коронарной болезни и связанных с ней осложнений, особенно сердечной недостаточности, остаётся перспективным направлением, изучение которого обеспечит понимание патофизиологии этого заболевания и определение новых целей для терапии. Одним из таких потенциальных биомаркеров является растворимый белок подавления онкогенности 2, который способен не только прогнозировать ремоделирование левого желудочка и неблагоприятный клинический исход среди пациентов с острым коронарным синдромом, но и дополнять другие, хорошо зарекомендовавшие себя сердечные биомаркеры, такие как натрийуретические пептиды и сердечные тропонины. В то же время, если в патогенез острой коронарной болезни вовлечён ряд отдельных, но часто сходящихся путей, то мультимаркерные подходы с различными комбинациями новых сердечных биомаркеров и их постоянная оценка, вероятно, улучшит прогнозирование сердечного риска и отдаленных исходов.
В статье представлены данные о частоте сочетания остеоартрита и сердечно-сосудистых заболеваний, особенностях их взаимоотношений, возможном влиянии препаратов, применяемых при лечении сердечно-сосудистых заболеваний, на развитие и прогрессирование остеоартрита.
В обзоре освещены вопросы распространенности, патогенеза и клинических проявлений бронхиальной астмы (БА), коморбидной с гастроэзофагеальной рефлюксной болезнью (ГЭРБ). Отмечены трудности диагностики триггеров экстраэзофагеальных симптомов. На основании большого количества клинических исследований в обзоре оценены возможности малоинвазивных методик выявления биомаркеров гастроэзофагеального рефлюкса (ГЭР) и дуоденогастроэзофагеального рефлюкса (ДГЭР) в ротовой жидкости. При синтропии ГЭРБ и БА отмечена значительная роль и связь параметров респираторного оксидативного воспаления с нарушениями функций внешнего дыхания. Для подтверждения рефлюксного происхождения экстраэзофагеальных респираторных симптомов актуально применение малоинвазивных методик выявления билирубина и пепсина в ротовой жидкости, а для оценки активности респираторного стресса - определение его субстратов в крови. Дальнейшие исследования, направленные на определение нормативных концентраций субстратов ДГЭР в ротовой жидкости и маркеров оксидативного респираторного воспаления в крови, будут способствовать улучшению диагностики и терапии при синтропии БА и ГЭРБ в амбулаторной практике.
Ишемический инсульт (ИИ) остается наиболее распространённой неврологической патологией [1,2] и может проявляться в форме злокачественного ишемического инсульта (ЗИИ), приводящего не только к тяжёлой инвалидизации пациента, но и к жизнеугрожающим состояниям [3,4]. Злокачественный ишемический инсульт — одно из наиболее грозных проявлений ишемического инсульта, угрожающее инвалидизацией трудоспособного населения и вероятностью летального исхода без назначения своевременной тактики лечения. Постановка диагноза «Злокачественный ишемический инсульт» может осуществиться не ранее 12–24 часов, за это время в головном мозге могут происходить необратимые изменения головного мозга, сопровождающиеся его выраженным отёком, с угрозой последующего вклинения, поэтому назначение адекватной и своевременной тактики лечения необходимо в кратчайшие сроки [5,6]. Учитывая особенности течения заболевания, возникает необходимость в поиске предикторов ЗИИ. С целью своевременного прогнозирования необратимых последствий в приведённом обзоре литературы мы рассматриваем современные подходы к диагностике злокачественного течения ишемического инсульта. Проводимый анализ литературных данных позволяет определить некоторые клинико-лабораторные предикторы развития злокачественного ишемического инсульта и способы оценки тяжести ишемического инсульта. Рассмотрены различные возможности применения исследуемых маркеров с целью практического использования в ранней диагностике ЗИИ. На основании данных литературы проанализированы возможности диагностики, с целью назначения своевременной и адекватной терапии до наступления необратимых изменений головного мозга.
ОРИГИНАЛЬНЫЕ ИССЛЕДОВАНИЯ
Цель: провести сравнительный анализ особенностей клинического, инструментального и лабораторного статуса пациентов с аортокоронарным шунтированием в анамнезе, перенёсших COVID-19. Материалы и методы: обследованы 42 пациента, прооперированных в ГБУЗ НО «НИИ – СККБ им. ак. Б.А. Королева» в 2019 г. Исследование проводилось в соответствии с принципами Хельсинской Декларации. От всех пациентов получено информированное добровольное согласие. Разделение пациентов на болевших и не болевших COVID-19 происходило на основании данных анализа мазка из носо- и ротоглотки, титра антител к вирусу SARS-CoV-2. Статистическая обработка выполнялась в программе Jamovi. Результаты: у перенёсших COVID-19 по сравнению с не болевшими уровень общего холестерина (ОХС) в крови был выше: 5,22 [4,03; 6,22] против 4.06 [3,56; 4,88] ммоль/л, р = 0,005; ОШ 0,492 [0,282; 0,858] 95% ДИ, p ratio 0,012.; уровень липопротеидов низкой плотности (ЛПНП) в крови был выше: 3,27 [2,16; 3,96] против 2,28 [1,60; 3,08] ммоль/л, p 0,014; ОШ 0,518 [0,294; 0,914] 95% ДИ, p ratio 0,023; чаще отмечалось ожирение: 15 (35,7%) против 9 (21,4%), p 0,009; ОШ 0,171 [0,0429; 0,685] 95% ДИ, p ratio 0,013; чаще встречалась хроническая болезнь почек (ХБП) С3а стадии – 7 (16,7%) против 1 (2,4%), p 0,008; ОШ 0,0779 [0,00855; 0,710] 95% ДИ, p ratio 0,024; отмечена тенденция к более высокому уровню креатинина — 89,7 [83,0; 105,0] против 81,0 [75,0; 90,5] мкмоль/л, p 0,060; ОШ 0,976 [0,945; 1,01] 95% ДИ, p ratio 0,153; тенденция к сниженной скорости клубочковой фильтрации (СКФ) по CKD-EPI: 66,1 ± 17,3 против 75,7 ± 16,1 мл/мин./1,73м2, p 0,034; ОШ 1,0368 [0,9962; 1,08] 95% ДИ, p ratio 0,076; тенденция к повышенному уровню Д-димера: 154 [104; 364] против 137 [97; 173] нг/мл, p 0,07; ОШ 0,997 [0,994; 1,0] 95% ДИ, p ratio 0,141; тенденция к более высокой средней суточной ЧСС: 75 [71; 79,5] против 72 [63; 74,5] уд./мин., p 0,026; ОШ 0,951 [0,886; 1,02] 95% ДИ, p ratio 0,169. При оценке вариабельности сердечного ритма статистически значимой разницы не получено. Заключение: исследование выявило ряд изменений лабораторных и инструментальных данных у пациентов с АКШ в анамнезе, переболевших COVID-19, а именно высокий уровень ОХС и ЛПНП в крови, тенденцию к сохранению повышенного уровня Д-димера, к более высокому уровню креатинина в крови и более низкой СКФ, к сохранению более высокой средней ЧСС. Требуется более тщательный контроль за этими показателями с своевременной коррекцией терапии.
Цель: изучить уровень молекулы адгезии сосудистого эндотелия 1 типа у пациентов с ишемической болезнью сердца и хронической болезнью почек, определить возможность использования данного маркера в качестве предиктора прогрессирования сердечно-сосудистых заболеваний. Материалы и методы: в исследование включены 115 пациентов с ишемической болезнью сердца (ИБС), стабильной стенокардией (напряжения), функциональный класс 1–3, хронической болезнью почек (ХБП) C1–C3, средний возраст составил 67,56 ± 12,42 лет (63 мужчины, 52 женщины). Проведена оценка уровня молекулы адгезии сосудистого эндотелия 1 типа (VCAM 1) с помощью иммуноферментного набора для количественного определения человеческого VCAM 1 ThermoFisher scientific. Результаты: у пациентов с ИБС и ХБП уровень сывороточного VCAM1 прогрессивно увеличивается по мере утяжеления ФК стенокардии и может расцениваться как ранний маркер прогрессирования ИБС. Уровень VCAM1 не зависит от стадии ХБП. При изучении корреляционных взаимосвязей между уровнем сывороточного VCAM1 и клинико-лабораторными данными было установлено, что имеется корреляционная взаимосвязь между VCAM1 и уровнем САД и ДАД. Заключение: для выявления пациентов с высоким риском сердечно-сосудистых осложнений при ИБС и ХБП целесообразно использовать определение уровня VCAM 1.
Цель: изучить клинические характеристики пациентов с фенотипом брохиальной астмы с ожирением в сочетании с хронической ишемической болезнью сердца. Материал и методы: в процессе открытого клинического исследования были сформированы две группы пациентов с хронической ишемической болезнью сердца (ХИБС) и бронхиальной астмой (БА). Пациенты I группы (n=43) имели в качестве сопутствующего заболевания ожирение. Группу II (n=50) составили пациенты без ожирения. Всем пациентам было проведено общеклиническое обследование. Оценены результаты холтеровского суточного мониторирования электрокардиограммы (ХМЭКГ), дуплексного сканирования брахиоцефальных артерий (ДС БЦА), трансторакальной эхокардиографии (ЭхоКГ), коронароангиографии (КАГ), спирографии. Также оценены результаты биохимического исследования крови. Результаты: для пациентов I группы основными жалобами оказались одышка (84% против 62%, р=0,036) и кашель (65% против 40%, р=0,027) в сравнении с пациентами контрольной группы. По результатам ЭХО-КГ в данной группе выявлены признаки перегрузки левых отделов сердца. Показатель КДО ЛЖ оказался более значимым, чем у пациентов контрольной группы (р=0,034). Толщина МЖП также более значима у пациентов I группы (р=0,022). По результатам УЗИ общей сонной и внутренней сонной артерий выявлены атеросклеротические бляшки у 53% пациентов группы I против 30% (р=0,037) контрольной группы. Согласно данным КАГ, распространённость стеноза ПКА оказалась более значимой у пациентов группы I (56% против 24%, р=0,003). У пациентов группы I по результатам спирометрии выявлено более выраженное снижение показателя ОФВ1 (64,1±6,7 против 66,9±7,1, р=0,042). Заключение: для фенотипа БА с ожирением в сочетании с ХИБС характерны более частые жалобы на кашель как эквивалент удушья при бронхообструктивном синдроме. Также пациенты чаще отмечают одышку как эквивалент боли при стенокардии и, возможно, проявление дыхательной и сердечной недостаточности. Эти клинические особенности фенотипа находят отражение в результатах инструментальных методов обследования: выраженное атеросклеротическое поражение сосудов, признаки перегрузки левых отделов сердца, более значимое снижение показателя ОФВ1.
Цели: установить прогностические маркеры неэффективности двойной антигипертензивной терапии у пациентов с артериальной гипертензией (АГ) высокого и очень высокого сердечно-сосудистого риска, построить модель прогнозирования отрицательного исхода двойной гипотензивной терапии. Материалы и методы: обследовано 88 больных с неконтролируемым течением АГ, не получавших базисную антигипертензивную терапию, средний возраст —58,0±1,52 лет. Обследование проводилось на основании действующих нормативных документов, регламентирующих ведение на стационарном этапе. Дополнительно определялся уровень высокочувствительного С-реактивного белка, уратов крови. Проводился суточный мониторинг артериального давления (СМАД) и электрокардиограммы (ЭКГ), респираторная полиграфия сна, компьютерная капилляроскопия. Поиск предикторов и построение прогностической модели проводились с использованием метода бинарной логистической регрессии. Результаты: эффективность двойной медикаментозной терапии составила 33,0%. Выделены прогностические маркеры, ассоциированные с отрицательным исходом лечения: толщина межжелудочковой перегородки (МЖП) (ОШ 3,44; р=0,009), линейная плотность капиллярной сети (ОШ 4,65, р<0,001), площадная плотность капиллярной сети (ОШ 3,98; р<0,001), ширина периваскулярной зоны (ОШ 6,04; р=0,002), диаметр артериального отдела (ОШ 2,86; р=0,007), диаметр переходного отдела капилляра (ОШ 3,59; р=0,005), коэффициент ремоделирования (ОШ 8,40; р=0,003), средненочное систолическое артериальное давление (САД) (ОШ 1,94; р=0,014), среднесуточное САД (ОШ 2,86; р=0,014), SDNNi (ОШ 2,86; р=0,007). В итоговую модель вошли толщина МЖП, площадная плотность капиллярной сети, среднесуточное САД. Характеристики модели: регрессионный коэффициент 25,74; р<0,001; p Вальда 0,049; ОШ 9,1 (95% ДИ 3,12; 26,82). Чувствительность метода составила 83,1%, специфичность — 69,0%. Площадь под ROC-кривой составила 0,805±0,05 (95% ДИ 0,707; 0,882). Точка cut-off соответствовала значению расчетной вероятности 0,599. Заключение: продемонстрирована низкая эффективность двойной антигипертензивной терапии. С учётом отсутствия утвержденных алгоритмов прогнозирования исходов медикаментозного лечения у пациентов с неконтролируемой АГ разработанная модель представляет клинический интерес и может быть полезна в достижении лучшего контроля АД. Для улучшения качества модели в целях увеличения чувствительности и специфичности метода требуется дальнейшее изучение на выборках большего объема.
Цель: провести сравнительный анализ динамики изменения конечных продуктов гликолиза и изоформного состава гигантского белка (титина и небулина) в скелетной и сердечной мышцах животных с гиперхолестеринемией (ГХ) на фоне длительного введения симвастатина. Материалы и методы: исследование проводилось на крысах, которых в течение трёх месяцев содержали на высокожировом и высокоуглеводном рационе. После подтверждения ГХ животных разделили на группы: I группа получала только экспериментальный рацион; II группа два месяца получала симвастатин в виде водной суспензии из расчета 0,012 г/кг массы животного один раз в сутки. Контрольная группа животных, содержалась на общем рационе вивария. Результаты: формирование ГХ сопровождалось накоплением пирувата и молочной кислоты как в миокарде, так и в мышечной ткани. Выявленные метаболические изменения отражают структурные нарушения и свидетельствуют о формировании гипоксии. На фоне введения симвастатина как в миокарде, так и в скелетной мускулатуре отмечено уменьшение уровня пирувата и молочной кислоты и приближение этих показателей к значениям контрольной группы. Такие изменения отражают тенденцию к восстановлению интеграции внутриклеточных метаболических процессов. Однако при исследовании белков титина и небулина на фоне применения симвастатина как в миокарде, так и в скелетных мышцах были отмечены структурные изменения: накопление протеолитического Т-фрагмента, снижение содержания изоформ интактного титина. Также статин-индуцированные структурные нарушения были выявлены в более ранних исследованиях биоптатов мышечной ткани крыс. Заключение: проведённое сравнительное исследование наглядно демонстрирует, что миокард наряду со скелетной мускулатурой является органом-мишенью токсического действия статинов. Исходя из этого данные, полученные в результате исследования, важно учитывать при фармакотерапии статинами.
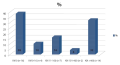
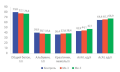
Цель: изучить особенности коронарной кальцификации у пациентов с хронической болезнью почек, получающих заместительную почечную терапию программным гемодиализом. Материалы и методы: в процессе открытого клинического исследования сформирована группа пациентов (n=43) с терминальной стадией хронической болезни почек (23 женщины и 20 мужчин). Средний возраст пациентов составил 54±13 лет, медиана стажа диализной терапии — 11 [6; 16] месяцев. Все пациенты получали заместительную почечную терапию программным гемодиализом. Процедуры проводили на аппаратах «искусственная почка» по стандартной схеме 3 раза в неделю по 4 часа. Пациентам проведено традиционное клинико-лабораторное обследование. У всех пациентов была оценена степень кальцификации коронарных артерий методом мультиспиральной компьютерной томографии. По шкале Агатстона проведена оценка тяжести коронарной кальцификации с учетом плотности и площади отложения кальция. Результаты: по результатам мультиспиральной компьютерной томографии для определения степени кальцификации коронарных артерий нами установлено, что у 48% пациентов определялся низкий и минимальный кальциноз, у 16% — незначительная кальцификация, у 36% — умеренная и выраженная кальцификация. При сравнении лабораторных показателей в группах пациентов с различной кальцификацией коронарных артерий у пациентов с незначительной, умеренной и выраженной кальцификацией уровень неорганического фосфора (1,64±0,07 ммоль/л) оказался значимо выше, чем у пациентов с минимальным и низким кальцинозом (1,35±0,12 ммоль/л) (р=0,04). Установлена выраженная прямая корреляционная зависимость между возрастом и показателем кальциевого индекса (r=0,52, p=0,0011). При увеличении стажа диализа отмечается увеличение кальциевого индекса (r=0,14; р= 0,045). Заключение: у 52 % пациентов с терминальной стадией хронической болезни почек, получающих заместительную почечную терапию программным гемодиализом, по результатам мультиспиральной компьютерной томографии коронарных артерий определяется коронарная кальцификация. Пациенты с незначительным, умеренным и выраженным кальцинозом коронарных артерий имеют значимо более выраженный уровень сывороточного фосфора в сравнении с пациентами с минимальным и низким кальцинозом (р<0,05). При этом возраст пациентов и стаж диализной терапии оказывают влияние на выраженность коронарного кальциноза.
Цель: изучить иммунные механизмы воспаления у пациентов с бронхиальной астмой (БА) в ассоциации с сахарным диабетом (СД) 2-го типа. Материалы и методы: исследованию подлежали 215 пациентов с персистирующей БА средней степени тяжести (средний возраст — 28,6±2,4 лет, 88 (40,9%) мужчин, 127 (59,1%) женщин. Среди обследованных больных было 64 человека с БА (I группа), 151 человек с БА в ассоциации с СД 2 типа (II группа), у которых наряду с рутинными лабораторными и инструментальными методами использовали определение показателей клеточного иммунитета, уровня IgE и лимфоцитарных аутоантител. Результаты: у пациентов с БА в сочетании с СД 2 типа чаще отмечается неконтролируемое течение заболевания с осложнением в виде дыхательной недостаточности II степени. У пациентов с БА, а также при сочетании БА с СД 2 типа было отмечено формирование вторичного иммунодефицита за счет клеточного звена. Сочетание БА и СД 2 типа характеризуется наиболее выраженными негативными изменениями клеточного иммунитета среди всех обследованных пациентов. При БА в сочетании с СД 2 типа отмечено снижение концентрации IgE наряду с увеличением количества лимфоцитарных аутоантител. Выводы: у больных БА в сочетании с СД 2 типа отмечается более тяжёлое течение БА и присоединение к аллергическому воспалению более деструктивного (аутоиммунного), что повышает риск развития осложнений обоих заболеваний.
Цель: изучение распространения синдрома тревоги у пациентов с хроническими неинфекционными заболеваниями (ХНИЗ) в амбулаторной практике. Материалы и методы: включены лица обоего пола старше 18 лет, посещавшие амбулаторно-поликлинические учреждения крупного промышленного центра Восточной Сибири летом 2022 г. Диагнозы ХНИЗ были установлены согласно современным клиническим рекомендациям. Обследованные были разделены на две группы. В первую группу включены лица без ХНИЗ, во вторую группу вошли пациенты с сопутствующими ХНИЗ. Оценка психоэмоционального состояния выполнялась с помощью теста Спилбергера-Ханина с раздельным определением уровней личностной и ситуативной тревоги. Статистический анализ данных проводился с помощью пакета прикладных программ Statistica 12.0 (StatSoft Inc., США). Результаты: уровень ситуативной тревоги у пациентов с ХНИЗ был статистически значимо выше в сравнении с лицами без сопутствующей соматической патологии. У пациентов с ХНИЗ в сравнении с лицами без таковых выявлено значимое повышение медианы баллов по уровню низкой и умеренно выраженной личностной тревоги и по уровню умеренной и высокой ситуативной тревоги. В группе пациентов с ХНИЗ достоверно чаще отмечался высокий уровень личностной и ситуативной тревоги в сравнении с лицами без ХНИЗ. Заключение: распространённость тревожного синдрома, в особенности ситуативной тревоги у пациентов с ХНИЗ в амбулаторно-поликлинической сети достаточно высока и достигает 93%, что требует решения вопроса о практической психиатрической помощи данным пациентам.
Цель: оценка субхронической токсичности бис-(3,5-ди-трет-бутил-4-гидроксифенил)тиолат диметилолова (Ме-3) и (3,5-ди-трет-бутил-4-гидроксифенил)тиолат трифенилолова (Ме-5) с выявлением внешних признаков токсичности и изменением показателей функционального состояния печени и почек крыс линии Wistar (самки) при 14-кратном ежедневном внутрижелудочном введении для моделирования метрономного режима химиотерапии. Материалы и методы: исследование проведено на 24 крысах Wistar (самки) весом 190–210 г. Тестируемые соединения вводили четырнадцатикратно ежедневно внутрижелудочно в суммарной дозе для Ме-3 2000 мг/кг, для Ме-5 - 954 мг/кг. Результаты: для субстанций, относящихся к классу органических производных олова, выявлены особенности протекания токсического процесса и показатели функционального состояния органов детоксикации (печень и почки) при субхроническом введении. Введение в суммарных дозах, составляющих полулетальную дозу при четырнадцатикратном введении, не вызвало гибели животных и развития внешних признаков токсичности. Изменение показателей функционального состояния печени и почек не отмечено. Вывод: анализ результатов исследования позволит разработать оптимальные схемы введения оловоорганических соединений, содержащих фрагмент 2,6-ди-трет-бутилфенола, в метрономном режиме химиотерапии.
КЛИНИЧЕСКИЕ СЛУЧАИ
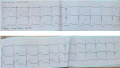
Феохромоцитома (ФХ) — опухоль из хромаффинных клеток симпато-адреналовой системы, продуцирующая большое количество катехоламинов (адреналин, норадреналин, дофамин). В литературе отсутствуют достоверные данные о частоте кардиальных проявлений феохромоцитомы, что связано с редкостью данной патологии. Данный случай демонстрирует развитие катехоламин-индуцированной кардиомиопатии, протекающей под маской инфаркта миокарда как первичное проявление феохромоцитомы. Пациентка была направлена с диагнозом «Ишемическая болезнь сердца, инфаркт миокарда» для выполнения коронароангиографии, по результату исследования патологии коронарных артерий не выявлено. В процессе дообследования выявлена феохромоцитома левого надпочечника. Первоначальные изменения электрокардиограммы, эхокардиографического исследования, лабораторных показателей регрессировали, что подтверждало развитие кардиомиопатии, развившейся на фоне феохромоцитомы. В настоящее время возрастает количество сведений о неишемическом поражении миокарда у пациентов с феохромоцитомой. Эти изменения в виде клинических появлений (боли за грудиной, одышка, различные виды аритмий), а также неспецифических изменений, по данным ЭКГ, нарушений локальной кинетики со снижением глобальной сократимости миокарда без стенотического поражения КА получили название катехоламин-индуцированной кардиомиопатии.
В настоящее время отмечается рост числа публикаций, посвящённых проблеме первично-множественных опухолей — новообразований, возникающих одновременно (синхронно) или поочередно (метахронно), развивающихся самостоятельно и независимо друг от друга в пределах одного или разных органов. Они описаны в виде двух, трёх и более нозологий. В связи с наличием дефектов иммунной системы при хроническом лимфолейкозе частой находкой являются солидные опухоли разных локализацией. Их развитие возможно и при других гематологических заболеваниях. Вероятно, это обусловлено успехами в излечении опухолевых заболеваний, увеличением продолжительности жизни пациентов, урбанизацией, возрастанием интенсивности канцерогенных техногенных, лекарственных воздействий, наличием первичных и вторичных иммунодефицитов, а также использованием современных методов диагностики. Одновременное выявление миелопролиферативного и лимфопролиферативного заболеваний у пациента встречается редко (в 1%), и это влечет за собой трудности в диагностике и назначении терапии при такой ассоциации. В связи с этим необходима настороженность при наличии клинических и лабораторных признаков заболевания системы крови, не характерных для установленного типа гемобластоза. И, безусловно, несомненный интерес представляет собственный опыт ведения таких пациентов.
СТРАНИЦЫ ИСТОРИИ
Прародителем Ростовского государственного медицинского университета (РостГМУ) по праву можно считать Императорский Варшавский университет (ИВУ). У истоков образования кафедры госпитальной терапии в Варшаве стоял опытный интернист и прогрессивный ученый Андреев Николай Агапиевич (1836-1883 гг.) — патолог и терапевт, член-корреспондент Императорского Виленского медицинского общества, действительный статский советник, доктор медицины, профессор, заведующий кафедрой с 1870 по 1875 гг. Настоящая статья посвящена его светлой памяти и приурочена к 140-летию со дня смерти одного из отцов-основателей кафедры госпитальной терапии РостГМУ.